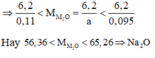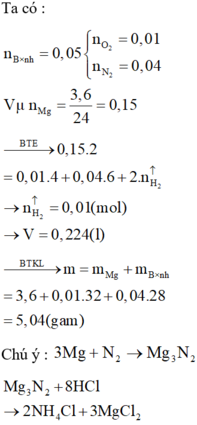cho 13,6g hỗn hợp 2 kim loại đồng và magie vào 36,5g dung dịch HCl 20% để phản ứng xảy ra hoàn toàn . Sau phản ứng thử dung dịch bằng quỳ tím thấy quỳ tím không chuyển màu. Trong dung dịch có một lượt chất rắn không tan . Lọc chất rắn này đem rửa sạch, nung trong không khí đến khi khối lượng thu được 16g oxit . Tính khối lượng mỗi kim loại trong hỗn hợp đầu