Trong 9,8g axit sunfuric có bao nhiêu Mol, bao nhiêu phân tử? Bao nhiêu mol nguyên tử hidro, lưu huỳnh, oxit; bao nhiêu nguyên tử hidro, lưu huỳn, oxit. Phải lấy bao nhiêu gam kim loại natri để số nguyên tử natri nhiều gấp 2 lần số nguyên tử S có trong axit?
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


Bài 1:
a) Số nguyên tử Al: 2. 6.1023=12.1023 (nguyên tử)
b) Số nguyên tử S: 0,1.6.1023= 6.1022 (nguyên tử)
c) nH2O=18/18=1(mol)
=> Tổng số mol nguyên tử: 2.1+1=3(mol)
Số nguyên tử trong 18 gam H2O: 3.6.1023=18.1023 (nguyên tử)
d) nHNO3= 6,3/63=0,1(mol)
Số mol nguyên tử trong 6,3 gam HNO3: 0,1.1+0,1.1+0,1.3=0,5(mol)
Số nguyên tử trong 6,3 gam HNO3: 0,5.6.1023=3.1023 (nguyên tử)
Bài 2:
nNaOH=20/40= 0,5(mol)
Số phân tử NaOH: 0,5.6.1023=3.1023 (phân tử)
Số phân tử H2O= Số phân tử NaOH
<=> nH2O=nNaOH=0,5(mol)
=> mH2O=0,5.18=9(g)


\(M_H=98-32-16.4=2\left(đvC\right)\)
⇒ Có 2:1 = 2 ntử H trong 1 ptử H2SO4

Nếu có có 6 , 02 . 10 23 nguyên tử Al sẽ tác dụng với:
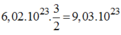 phân tử
H
2
S
O
4
phân tử
H
2
S
O
4
Và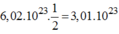 phân tử
A
l
2
S
O
4
3
phân tử
A
l
2
S
O
4
3
Tạo ra: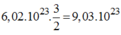 phân tử
H
2
phân tử
H
2

Số lưu huỳnh bị khử :0->+4 (+4)
Số lưu huỳnh bị oxi hóa:+6->+4 (-2)

Trong 16g khí oxi có 16/16 = 1 mol nguyên tử oxi và 16/32 = 0,5 mol phân tử oxi

\(1s^22s^22p^63s^23p^4\)
Nguyên tử lưu huỳnh có 16e.
Số hiệu nguyên tử của lưu huỳnh là 16.
Lớp thứ 3 có mức năng lượng cao nhất.
Nguyên tử lưu huỳnh có 3 lớp:
- Lớp thứ nhất có 2e.
- Lớp thứ hai có 8e.
- Lớp thứ ba có 6e.
Lưu huỳnh là phi kim vì có 6e lớp ngoài cùng.

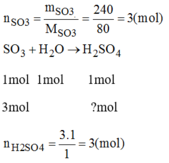

cái này là hoá bạn đừng đăng vào online math bạn đăng câu hỏi vào link này nhé:
https://h.vn/
@Út Nhỏ Jenny: làm gì có link này c nhỉ???