Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đặt công thức của oxit kim loại là MxOy
%mO = 100% - 70% = 30%
⇒ mO = 12y = 160.30% = 48
⇒ y = 3
mM = 160.70% = 112g = M.x (với M là phân tử khối của kim loại M)
Áp dụng quy tắc hóa trị ta có:
a.x = 2.3 = 6 (với a là hóa trị của M; a = 1; 2; 3)
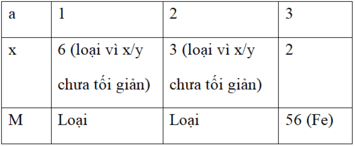
⇒ M là kim loại Sắt.
Vậy công thức hóa học của oxit kim loại là Fe2O3 (Sắt (III) oxit).

\(m_{KL}=\dfrac{70.160}{100}=112\left(g\right)\)
\(m_O=160-112=48\left(g\right)\)
=> Số nguyên tử O = \(\dfrac{48}{16}=3\) (nguyên tử)
CTHH của oxit có dạng AxO3
=> x.NTKA = 112
Chỉ có x = 2 thỏa mãn => NTKA = 56 (đvC)
=> A là Fe
CTHH: Fe2O3

Cái đề hình như sai sửa lại xíu :Cho biết khối lượng mol một oxit kim loại là 160g. thành phần về khối lượng của kim loại trong oxit đó là 70%. Lập công thức hóa học của oxit. Gọi tên oxít đó. (Nếu đề không sai thì kq không đẹp)
Đặt CTHH của oxit là : \(M_xO_y\).
Theo bài ra ta có ;
\(M_M=160\dfrac{g}{mol}\)
mO=160.30%=48(g)-> nO= 3mol
\(\Rightarrow\) số nguyên tử tử oxi trong oxit kim loại là 3 nguyên tử oxi.
Vậy công thức hoá của oxit là \(M_2O_3.\)
mà \(m_A=\dfrac{160.70}{100}=112g\)
M = \(\dfrac{112}{x}\)
x = 1 => M = 112 (loại)
x = 2 => M = 56 (nhận)
x = 3 => M = 37,3 (loại)
\(\rightarrow M_A=\dfrac{112}{2}=56g\)
Vậy kim loại đó là Fe .
\(\Rightarrow CTHH:Fe_2O_3\)
Gọi tên : Sắt (III) oxit .
Gọi công thức của oxit đó là MxOy
Ta có Mx/(Mx + 16y) = 70/100
Mà Mx + 16y = 160 => Mx = (70/100).160 = 112g => M = 112/x
Với x = 2 => M = 56 (Fe)
x = 2 => y = (160 - 56.2)/16 = 3
Vậy oxit kim loại có công thức là Fe2O3 (Sắt (III) oxit)
* Nói thêm một chút tại sao x = 2 : cái này do mình làm tắt đó thôi, chứ đúng ra phải biện luận thế này nè :
M = 112/x
x = 1 => M = 112 (loại)
x = 2 => M = 56 (Fe)
x = 3 => M = 37,3 (loại)

Gọi CTHH của oxit kim loại là RxOy
Ta có:\(m_O=94.\left(100\%-82,98\%\right)=16\left(g\right)\Rightarrow y=\dfrac{16}{16}=1\)
\(\Rightarrow m_R=94-16=78\left(g\right)\)
\(\Rightarrow M_R=\dfrac{78}{x}\left(đvC\right)\)
Vì R là kim loại nên có hóa trị l,ll,lll
| x | l | ll | lll |
| MR | 78 | 39 | 26 |
| Kết luận | loại | thỏa mãn | loại |
⇒ R là kali (K)
Vậy CTHH là K2O

Gọi CT tổng quát của oxit kim loại cần tìm là FexOy (x,y: nguyên, dương)
Ta có: %mO= 100% - %mFe= 100% - 70%= 30%
=> mO= 160. 30/100= 48(g)
=> nO= 48/16=3(mol)
mFe= 160.70/100= 112(g)
=> nFe= 112/56= 2(mol)
Vậy: CTHH là Fe2O3 (sắt (III) oxit)
Gọi công thức của oxit đó là MxOy
Ta có \(\dfrac{M_x}{M_x+16_y}=\dfrac{70}{100}\)
Mà Mx + 16y = 160 => Mx = \(\dfrac{70}{100}\).160 = 112g =>
M = \(\dfrac{112}{x}\)\(\left\{{}\begin{matrix}x=1\Rightarrow M=112\\x=2\Rightarrow M=56\\x=3\Rightarrow M=37,3\end{matrix}\right.\)
Với x = 2 => M = 56 (Fe)
x = 2 => y = \(\dfrac{160-56.2}{16}\) = 3
Vậy oxit kim loại có công thức là Fe2O3 (Sắt (III) oxit)
Cái này là mk tra bảng tuần hoàn nó là Cadimi nhưng cái này chưa học nên mk nghĩ là Fe nhưng thật ra chắc là Cadimi



Khối lượng của kim loại có trong oxit kim loại:
MKL = 112 g
Khối lượng nguyên tố oxi: mO = 160 – 112 = 48g
Đặt công thức hóa học của oxit kim loại là MxOy, ta có:
MKL. x = 112 => nếu x = 2 thì M = 56. Vậy M là Fe
16y = 48 => y = 3
Vậy CTHH: Fe2O3, đó là sắt (III) oxit
Gọi Công thức hóa học của oxit đó là : MxOy
Ta có : khối lượng của M trong 1 mol là : 160 . 70 : 100 = 112(g)
=> khối lượng của Oxi trong 1 mol là : 160 - 112 = 48(g)
=> số nguyên tử Oxi có trong 1 phân tử Oxit là : 48 : 16 = 3 (nguyên tử)
=>y = 3 => M có hóa trị là III
Ta có : III . x = 3 . II
=> x = 2
=> MxOy = M2O3
=> Mkim loại M là 112 : 2 = 56 (g/mol)
=> M = Fe
Vậy tên Oxit đó là : Fe2O3