Phân tích 0,58 gam một hợp chất hữu cơ X (chứa C, H, O) tìm được %C = 62,06; % H = 10,34. Vậy khối lượng oxi trong hợp chất X là
A. 0,08 gam.
B. 0,16 gam.
C. 0,09 gam.
D. 0,14 gam.
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

\(\%O=100-62,06-10,34=27,6\%\)
Ta có :
\(\%O=\frac{mO}{mhh}.100\%\Leftrightarrow27,6=\frac{mO}{0,29}.100\%\)
\(\rightarrow m_O=0,08g\)
Vậy chọn B

n CO2=11,0/44=0,25(mol)
=>n(C)=0,25mol
mC=0,25*12=3(g)
n H2O=6,75/18=0,375(mol)
=>nH=0,75(mol)
=>mH=0,75(g)
nO=2/16=0,125(mol)
CTPT là CxHyOz
x:y:z=0,25:0,75:0,125=2:6:1
=>C2H6O là CTĐGN
=>CTPT là \(C_{2x}H_{6x}O_x\)
Theo đề, ta có: 24x+6x+16x=46
=>x=1
=>C2H6O

Hợp chất X đơn chức tác dụng được với AgNO3/NH3 thu được bạc kết tủa nên X là anđehit đơn chức.
Gọi công thức phân tử của X là R-CHO
RCHO + 2AgNO3 + 3NH3 + H2O → RCOONH4 + 2Ag↓ + 2NH4NO3
Theo phương trình:
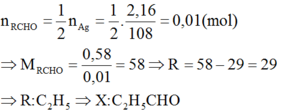
CTCT của X là: CH3-CH2-CHO (propanal)

\(n_{CO_2}=\dfrac{17,6}{44}=0,4\left(mol\right)\)
Bảo toàn C: nC = 0,4 (mol) => mC = 0,4.12 = 4,8(g)
\(n_{H_2O}=\dfrac{8,1}{18}=0,45\left(mol\right)\)
Bảo toàn H: nH = 0,9 (mol) => mH = 0,9.1 = 0,9 (g)
\(n_{N_2}=\dfrac{1,12}{22,4}=0,05\left(mol\right)\)
Bảo toàn N: nN = 0,1 (mol) => mN = 0,1.14 = 1,4 (g)

Chọn đáp án A
X → 180 g , 1 N a O H Y → H 2 O ↑
X → N a O H Y → Z N a 2 C O 2 + C O 2 + H 2 O
X → N a O H Y → Z R C O O H + T C , H , O , M T < 126
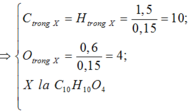
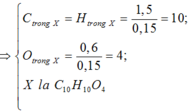
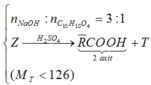
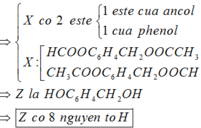
Chọn B
%O = 100 - %C - %H = 100 – 62,06 – 10,34 = 27,6 (%)
Khối lượng oxi trong hợp chất là: m O = 0,58.27,6% = 0,16008 (gam).