Phân bón A có chứa 90% Amôni sunfat (NH4)2SO4. Phân bón B có chứa 60% Amôni nitrat NH4NO3. Hỏi nếu cần bón cho ruộng 42 kg đạm (N) thì dùng A hay B sẽ nhẹ công vận chuyển hơn ?
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


Ta có:
Ca(NO3)2 có: \(\%N=\dfrac{14.2}{40+14.2+16.6}\approx17,07\%\)
NH4NO3 có : \(\%N=\dfrac{14.2}{14+4+14+16.3}=35\%\)
Nếu dùng Ca(NO3)2 : \(m_{Ca\left(NO_3\right)_2}=\dfrac{56}{17,07\%}=328\left(kg\right)\rightarrow m_A=\dfrac{328}{82\%\%2}=400\left(kg\right)\)
Nếu dùng NH4NO3: \(m_{NH_4NO_3}=\dfrac{56}{35\%}=160\left(kg\right)\rightarrow m_B=\dfrac{160}{80\%}=200\left(kg\right)\)
-> Mua phân B sẽ tốn ít công vận chuyển hơn vì nhẹ hơn ( 200 kg < 400 kg )

Ta có:
Ca(NO3)2 có %N=14x2/(40+14x2+16x6)≈17,07%
NH4NO3 có %N=14x2/(14+4+14+16x3)=35%
Nếu dùng Ca(NO3)2
mCa(NO3)2=56/17,07%=328 kg -> m A=328/82%=400kg
Nếu dùng NH4NO3
-> mNH4NO3=56/35%=160 kg -> mB=160/80%=200kg
-> mua phana B sẽ ít hơn đỡ tốn công vận chuyển hơn (400>200)

Trong 1 mol \(\left(NH_4\right)_2SO_4\) có 2 mol N.
Hay trong 132gam \(\left(NH_4\right)_2SO_4\) có 28gam N
Vậy trong x kg \(\left(NH_4\right)_2SO_4\) có 42 kg N
\(m_{\left(NH_4\right)_2SO_4}=x=\frac{42.132}{28}=198\left(kg\right)\)
\(\Rightarrow m_A=198:90\%=220\left(kg\right)\)
Trong 1 mol \(NH_4NO_3\) có 2 mol N
Hay trong 80gam \(NH_4NO_3\) có 28gam N
Vậy trong y kg \(NH_4NO_3\) có 42kg N
\(m_{NH_4NO_3}=y=\frac{42.80}{28}=120\left(kg\right)\)
\(\Rightarrow m_B=120:60\%=200\left(kg\right)\)
\(\Rightarrow m_A>m_B.\) Vậy dùng phân bón B nhẹ công vận chuyển hơn.

\(\%N\left(CO\left(NH_2\right)_2\right)=\dfrac{2.14}{60}.100\%=46,67\%\)
\(\%N\left(\left(NH_4\right)_2SO_4\right)=\dfrac{2.14}{132}.100\%=21,21\%\)
\(\%N\left(NH_4NO_3\right)=\dfrac{2.14}{80}.100\%=35\%\)
\(\%N\left(Ca\left(NO_3\right)_2\right)=\dfrac{2.14}{164}.100\%=17,07\%\)
=> CO(NH2)2 có hàm lượng N cao nhất
=> A

- Vì khi bón chung chúng sẽ sảy ra phản ứng gây giảm N do bị thoát khí NH3 ra.
- Các phản ứng sẽ xảy ra đó là :
\(2NH_4NO_3+Ca\left(OH\right)_2\rightarrow Ca\left(NO_3\right)_2+2NH_3+H_2O\)
\(2NH_4NO_3+K_2CO_3\rightarrow2KNO_3+2NH_3+H_2O+CO_2\)
\(\left(NH_4\right)_2SO_4+Ca\left(OH\right)_2\rightarrow CaSO_4+2NH_3+2H_2O\)
\(\left(NH_4\right)_2SO_4+K_2CO_3\rightarrow K_2SO_4+2NH_3+CO_2+H_2O\)
\(CO\left(NH_2\right)_2+Ca\left(OH\right)_2\rightarrow CaCO_2+2NH_3\)
\(CO\left(NH_2\right)_2+H_2O+K_2CO_3\rightarrow2KHCO_3+2NH_3\)
- Vì khi bón chung chúng sẽ sảy ra phản ứng gây giảm N do bị thoát khí NH3 ra.
- Các phản ứng sẽ xảy ra đó là :
2NH4NO3+Ca(OH)2→Ca(NO3)2+2NH3+H2O2NH4NO3+Ca(OH)2→Ca(NO3)2+2NH3+H2O
2NH4NO3+K2CO3→2KNO3+2NH3+H2O+CO22NH4NO3+K2CO3→2KNO3+2NH3+H2O+CO2
(NH4)2SO4+Ca(OH)2→CaSO4+2NH3+2H2O(NH4)2SO4+Ca(OH)2→CaSO4+2NH3+2H2O
(NH4)2SO4+K2CO3→K2SO4+2NH3+CO2+H2O(NH4)2SO4+K2CO3→K2SO4+2NH3+CO2+H2O
CO(NH2)2+Ca(OH)2→CaCO2+2NH3CO(NH2)2+Ca(OH)2→CaCO2+2NH3
CO(NH2)2+H2O+K2CO3→2KHCO3+2NH3
chúc bạn học tốt

10ha khoai tây cần 60. 10 = 600 kg nitơ
Bảo toàn nguyên tố Nito:
⇒ 1 mol (80g) NH4NO3 tạo thành 1 mol (28g)N2
Lượng NH4NO3 cần để có 600kg N2 là
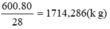
Phân đạm amoni nitrat chứa 97,5% NH4NO3 nên lượng phân đạm cần bón là:
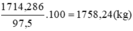


ta có : trong 100g phân bón A chứa 90 g (NH4)2SO4
132g (NH4)2SO4 chứa 28g N
90g (NH4)2SO4 chứa x g N
=>x=90 .28/132=19,38(g)
lượng đạm của phân bón A là 19,38(%)
nếu cần bón cho ruộng 42kg đạm thì lượng phân bón A cần dùng là :
19,38/100 .4200=813,96(g)
phân bón B làm tương tự ta được lượng đạm =10,5(%)
lượng phân bón B cần dùng để bón cho ruộng 42kg đạm là :
10,5/100.4200=441(g)
vậy dùng phân bón B sẽ nhẹ công vận chuyển hơn