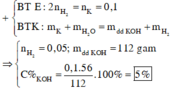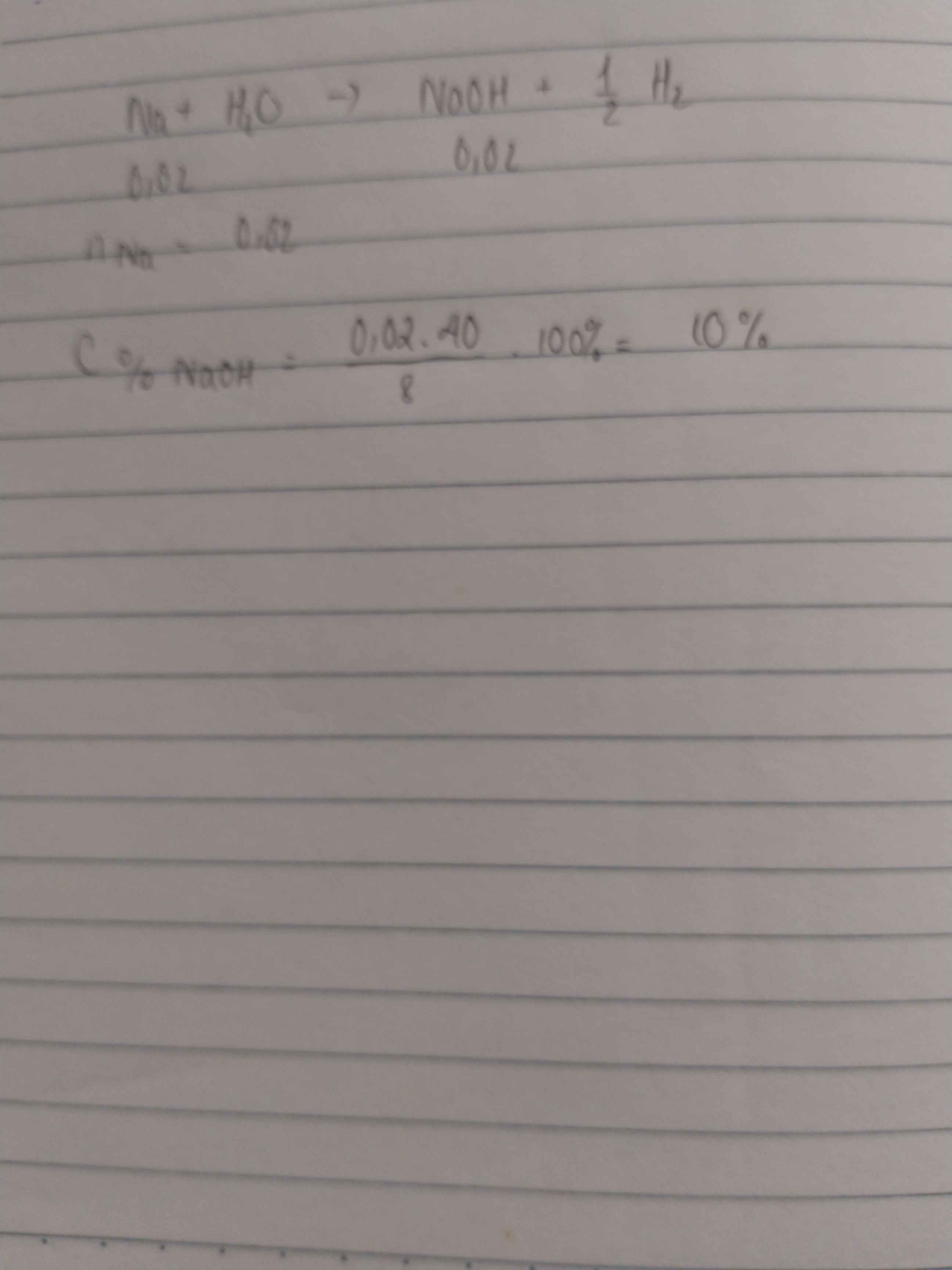nồng độ phần trăm của dung dịch thu được khi cho 3,9g kali tác dụng với 108,2g H2O là ?
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


\(n_K=\dfrac{3,9}{39}=0,1\left(mol\right)\)
PTHH: 2K + Cl2 --to--> 2KCl
0,1 0,05 0,1
\(\rightarrow m_{KCl}=0,1.74,5=7,45\left(g\right)\\ V_{Cl_2}=0,05.22,4=1,12\left(l\right)\\ C\%_{KCl}=\dfrac{7,45}{250}=2,98\%\)
a, \(n_K=\dfrac{3,9}{39}=0,1\left(mol\right)\)
2K + Cl2 ----> 2KCl
0,1 0,05 0,1
\(V_{Cl_2}=0,05.22,4=1,12\left(l\right)\)
b, \(m_{KCl}=0,1.74,5=7,45\left(g\right)\)
\(\Rightarrow C\%_{ddKCl}=\dfrac{7,45.100\%}{250}=2,98\%\)

\(n_K=\frac{3,9}{39}=0,1\left(mol\right)\)
PTHH: K + 2Cl\(\rightarrow\) KCl2
0,1 \(\rightarrow\) 0,05 (mol)
VCl= 0,05.35,5=1,775(l)
K hóa trị 1, Cl cũng hóa trị 1 mà lại có công thức KCl2 là sao???

a,\(n_{Na}=\dfrac{4,6}{23}=0,2\left(mol\right);n_K=\dfrac{3,9}{39}=0,1\left(mol\right)\)
PTHH: 2Na + 2H2O → 2NaOH + H2
Mol: 0,2 0,1
PTHH: 2K + 2H2O → 2KOH + H2
Mol: 0,1 0,05
b, \(n_{H_2}=0,1+0,05=0,15\left(mol\right)\)
\(V_{H_2}=0,15.22,4=3,36\left(l\right)\)
c,mdd sau pứ=4,6+3,9+91,5-0,15.2=99,7 (g)
\(\%m_{NaOH}=\dfrac{0,2.40.100\%}{99,7}=8,02\%\)
\(\%m_{KOH}=\dfrac{0,1.56.100\%}{99,7}=5,62\%\)
Bài 3 :
\(n_{Na}=\dfrac{4,6}{23}=0,2\left(mol\right)\)
\(n_K=\dfrac{3,9}{39}=0,1\left(mol\right)\)
a) Pt : \(2Na+2H_2O\rightarrow2NaOH+H_2|\)
2 2 2 1
0,2 0,2 0,1
\(2K+2H_2O\rightarrow2KOH+H_2|\)
2 2 2 1
0,1 0,1 0,05
b) \(n_{H2\left(tổng\right)}=0,1+0,05=0,15\left(mol\right)\)
\(V_{H2\left(dktc\right)}=0,15.22,4=3,36\left(l\right)\)
c) \(n_{NaOH}=\dfrac{0,1.2}{1}=0,2\left(mol\right)\)
⇒ \(m_{NaOH}=0,2.40=8\left(g\right)\)
\(n_{KOH}=\dfrac{0,05.2}{1}=0,1\left(mol\right)\)
⇒ \(m_{KOH}=0,1.56=5,6\left(g\right)\)
\(m_{ddspu}=8,5+91,5-\left(0,15.2\right)=99,7\left(g\right)\)
\(C_{NaOH}=\dfrac{8.100}{99,7}=8,02\)0/0
\(C_{KOH}=\dfrac{5,6.100}{99,7}=5,62\)0/0
Chúc bạn học tốt

Khối lượng dung dịch = 108,2 + 3,9 - 0,1 = 112 gam
Khối lượng chất tan = 0,1 x 56 = 5,6 gam
Nồng độ % = 5,6/112 = 0,05 = 5/100 = 5%

\(n_{H_2}=\dfrac{v}{22,4}=\dfrac{11,2}{22,4}=0,05mol\)
-Gọi A là kim loại kiềm
2A+2H2O\(\rightarrow\)2AOH+H2
\(n_A=2n_{H_2}=2.0,05=0,1mol\)
\(M_A=\dfrac{m_A}{n_A}=\dfrac{3,9}{0,1}=39\left(K\right)\)
\(n_{KOH}=n_K=0,1mol\rightarrow m_{KOH}=0,1.56=5,6gam\)
\(m_{dd}=m_K+m_{H_2O}-m_{H_2}=3,9+500-0,05.2=503,8gam\)
C%KOH=\(\dfrac{5,6.100}{503,8}\approx\)1,11%
-Gọi X là kim loại kiềm cần tìm
Ta có: \(n_{H_2}=\dfrac{1,12}{22,4}=0,05mol\)
PTHH: \(2X+2H_2O\rightarrow2XOH+H_2\)
=> 0,1mol 0,1mol 0,05mol
\(M_X=\dfrac{m}{n}=\dfrac{3,9}{0,1}=39\)
Vậy kim loại X cần tìm là Kali (K)
Ta có: \(m_{KOH}=0,1.\left(39+16+1\right)=5,9\left(g\right)\)
\(m_{ddKOH}=m_K+m_{H_2O}-m_{H_2}=3,9+500-\left(0,05.2\right)=503,8\left(g\right)\)
\(C\%=\dfrac{m_{KOH}}{m_{ddKOH}}.100\%=\dfrac{5,9}{503,8}.100\%\approx1,17\%\)

\(a,n_{CuO}=\dfrac{4}{80}=0,05\left(mol\right)\)
PTHH: \(CuO+2HCl\rightarrow CuCl_2+H_2O\)
0,05---->0,1------>0,1
\(\rightarrow x=C\%_{HCl}=\dfrac{0,1.36,5}{200}.100\%=1,825\%\)
\(b,\) PTHH: \(CuCl_2+2NaOH\rightarrow Cu\left(OH\right)_2\downarrow+2NaCl\)
0,05----->0,1-------->0,05----------->0,1
\(\rightarrow m_{ddNaOH}=\dfrac{0,1.40}{10\%}=40\left(g\right)\\ \rightarrow m_{dd\left(sau.pư\right)}=40+200+4-0,05.98=239,1\left(g\right)\)
\(\rightarrow C\%_{NaCl}=\dfrac{0,1.58,5}{239,1}.100\%=2,45\%\)
\(n_{CuO}=\dfrac{4}{80}=0,05\left(mol\right)\\
pthh:CuO+HCl\rightarrow CuCl_2+H_2O\)
0,05 0,05 0,05 0,05
\(x=C\%_{HCl}=\dfrac{0,05.36,5}{200}.100\%=0,9125\%\\
pthh:CuCl_2+2NaOH\rightarrow Cu\left(OH\right)_2+2NaCl\)