Bài 4: Một loại oxit có khối lượng là 160 g/mol trong đó kim loại chiếm
70%. Hãy xác định CTHH của oxit.
Bài 5: Cho 50g dung dịch natri hiđroxit (NaOH) tác dụng với 36,5g axit
clohđric (HCl) tạo thành natri clorua (NaCl) và nước. Tính khối lượng
NaCl tạo thành.
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Bài 4:
\(Đặt:Fe_xO_y\\ x=\dfrac{160.70\%}{56}=2\\ y=\dfrac{160-56.2}{16}=3\)
=> CTHH oxit sắt : Fe2O3
\(n_{HCl}=\dfrac{36,5}{36,5}=1\left(mol\right)\\ PTHH:NaOH+HCl\rightarrow NaCl+H_2O\\ 1...........1.........1.........1\left(mol\right)\\ \rightarrow m_{NaCl}=1.58,5=58,5\left(g\right)\)
(Số liệu 50 gam không dùng đến? Vì đề cho cái đó là dung dịch)

1 ) CAO +H2O => CA(OH)2 (1)
2K + 2H2O => 2KOH + H2(2)
n (H2) =1,12/22,4 =0,05
theo ptpư 2 : n(K) = 2n (h2) =2.0.05=0,1(mol)
=> m (K) =39.0,1=3,9 (g)
% K= 3,9/9,5 .100% =41,05%
%ca =100%-41,05%=58,95%
xo + 2hcl =>xcl2 +h2o
10,4/X+16 15,9/x+71
=> giải ra tìm đc X bằng bao nhiêu thì ra

Một bếp lửa chờn vờn sương sớm
Một bếp lửa ấp iu nồng đượm
Cháu thương bà biết mấy nắng mưa
Hình ảnh “bếp lửa” trong màn sương sớm đã được khắc họa giản dị nhưng rõ nét và sống động qua ba câu thơ. “Bếp lửa” có lúc sáng mãnh liệt, có lúc yếu, không định hình đã trở thành một đồ dùng, một hình ảnh gần gũi và quen thuộc trong cuộc sống hằng ngày của người dân Việt Nam. Đó không chỉ là nơi để đun nấu mà còn là nơi sum họp, ghi dấu những niềm vui, nỗi buồn của mọi gia đình. Điệp ngữ “một bếp lửa” cùng với các từ láy “chờn vờn”, “ấp iu” đã gợi nên sự ấm áp, đầy tình thương yêu như tấm lòng bà. Từ “ấp iu” gợi lên sự khéo léo của bàn tay bà khi bà nhóm bếp lửa, tấm lòng yêu thương, chi chút của bà đến con cháu. Trong hồi tưởng của cháu, hình ảnh người bà luôn hiện diện cùng bếp lửa qua bao năm tháng. Hình ảnh của bà hiện lên một cách nhẹ nhàng nhưng vô cùng đẹp đẽ trong trái tim người cháu, bà vẫn luôn nhóm bếp lửa mỗi sáng mỗi chiều suốt cả cuộc đời. Hình ảnh “bếp lửa” là biểu hiện cụ thể và sinh động về sự tần tảo, chăm sóc và yêu thương của người bà đối với con cháu trong mọi hoàn cảnh khó khăn, gian khổ. Trước sự hy sinh của bà, người cháu luôn “thương bà biết mấy nắng mưa”. Từ đó làm bật lên tình cảm sâu nặng của người cháu một cách thật tự nhiên, không thể tà xiết vì những “nắng mưa”, khó nhọc vất vả của cuộc đời bà. Từ “thương” diễn đạt rất chân thật mà giản dị không chút hoa mỹ tấm lòng yêu mến bà của cháu.

X2Oy +2yHCl----->2XCly+yH2O
mHCl=30.36,5/100=10,95g
nHCl=10,95/36,5=0,3 mol
nH2O=0,3/2=0,15 mol
mH2O=0,15.18=2,7g
Áp dụng đl bảo toàn khối lượng mXCly=13,35 g
cứ 1 mol X2Oy------> 2 mol XCly
2X+16y g------->2X+71y g
5,1g 13,35 g
------->X=9y
vì x là kim loại nên có y=1,2,3---> X=9.3=27 (al)

\(a,PTHH:2Na+2H_2O\rightarrow2NaOH+H_2\\ n_{Na}=\dfrac{2,3}{23}=0,1mol\\ n_{NaOH}=0,1.2=0,2mol\\ C_{M_{NaOH}}=\dfrac{0,2}{0,5}=0,4M\\ b,oxit.kl:RO\\ n_{RO}=\dfrac{2,4}{R+16}mol\\ n_{HCl}=\dfrac{30.7,3}{100.36,5}=0,06mol\\ RO+2HCl\rightarrow RCl_2+H_2O\\ \Rightarrow\dfrac{2,4}{R+16}=0,06:2\\ \Leftrightarrow R=64,Cu\)

Phản ứng chỉ tạo ra muối nitrat và nước, chứng tỏ n là hoá trị duy nhất của kim loại trong oxit. Đặt công thức của oxit kim loại là M 2 O n và nguyên tử khối của M là A.
Phương trình hoá học :
M 2 O n + 2n H N O 3 → 2 M ( N O 3 ) n + n H 2 O (1)
Theo phản ứng (1), khi tạo thành 1 mol [tức (A + 62n gam)] muối nitrat thì đồng thời tạo thành 0,5 mol (tức 9n gam) nước.
(A + 62n) gam muối nitrat - 9n gam nước
34 gam muối nitrat - 3,6 gam nước
Ta có tỉ lệ: 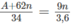
Giải phương trình được A = 23n. Chỉ có nghiệm n = 1, A = 23 là phù hợp. Vậy kim loại M trong oxit là natri.
Phản ứng giữa Na2O và HNO3:
Na2O + 2HNO3 → 2NaNO3 + H2O (2)
Theo phản ứng (2) :
Cứ tạo ra 18 gam H2O thì có 62 gam Na2O đã phản ứng
Vậy tạo ra 3,6 gam H2O thì có x gam Na2O đã phản ứng
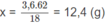

a) Đặt số mol của MO, M(OH)2, MCO3 tương ứng là x, y, z.
Nếu tạo muối trung hòa ta có các phản ứng:
MO + H2SO4 →MSO4 + H2O (1)
M(OH)2 + H2SO4 →MSO4 + 2H2O (2)
MCO3 + H2SO4 →MSO4 + H2O + CO2 (3)
Nếu tạo muối axít ta có các phản ứng:
MO + 2H2SO4 →M(HSO4)2 + H2O (4)
M(OH)2 + 2H2SO4 →M(HSO4)2 + 2H2O (5)
MCO3 + 2H2SO4 →M(HSO4)2 + H2O + CO2 (6)
Ta có :
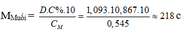
– TH1: Nếu muối là MSO4 M + 96 = 218 M = 122 (loại)
– TH2: Nếu là muối M(HSO4)2 M + 97.2 = 218 M = 24 (Mg)
Vậy xảy ra phản ứng (4, 5, 6) tạo muối Mg(HSO4)2
b) Theo (4, 5, 6) Số mol CO2 = 0,448/22,4 = 0,02 molz = 0,02 (I)
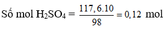
2x + 2y + 2z = 0,12 (II)
Đề bài: 40x + 58y + 84z = 3,64 (III)
Giải hệ (I, II, III): x = 0,02; y = 0,02; z = 0,02
%MgO = 40.0,02.100/3,64 = 21,98%
%Mg(OH)2 = 58.0,02.100/3,64 = 31,87%
%MgCO3 = 84.0,02.100/3,64 = 46,15%


Bài 4 :
Gọi CTHH của oxit là $Fe_xO_y$
Ta có :
\(\dfrac{56x}{70}=\dfrac{16y}{30}=\dfrac{160}{100}\). Suy ra : x = 2 ; y = 3
Vậy CTHH của oxit là $Fe_2O_3$
Bài 5 :
$n_{HCl} = \dfrac{36,5}{36,5} = 1(mol)$
$NaOH + HCl \to NaCl + H_2O$
Theo phương trình hóa học :
$n_{NaCl} = n_{HCl} = 1(mol)$
$m_{NaCl} = 58,5.1 = 58,5(gam)$