Cho 26 gam kim loại kẽm rác dụng hoàn toàn với lượng vừa đủ dung dịch axit clohydro (HCl). Sau phản ứng, thu được dung dịch chứa muối kẽm clorua (ZnCl2) và khí hydro ở điều kiện tiêu chuẩn (đktc).
a) tính thể tích hydro sinh ra ở đktc
b) khối lượng muối kẽm clorua thu được sau khi kết thúc phản ứng
c) hỏi tỉ lệ tổng khối lượng của các chất tham gia phản ứng so với các chất sản phẩm bằng bao nhiêu?
(Cho biết: Zn=65; H=1; Cl=35,5; Fe=56)


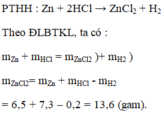

nZn = m/M = 26/65 = 0,4 (mol)
pthh: Zn + 2HCl -> ZnCl2 + H2
........1mol...2mol........1 mol.......1 mol
.......0,4mol..x mol........y mol........z mol
a, Từ ptpu ta có: \(n_{H_2}=z=\dfrac{0,4.1}{1}=0,4\left(mol\right)\)
=>\(V_{H_2}=n.22,4=0,4.22,4=8,96\left(l\right)\)
b, Từ ptpu ta có: \(n_{ZnCl_2}=y=\dfrac{0,4.1}{1}=0,4\left(mol\right)\)
=>\(m_{ZnCl_2}=n.M=0,4.\left(65+35,5.2\right)=0,4.136=54,4\left(g\right)\)
c, \(m_{H_2}=n.M=0,4.2=0,8\left(g\right)\)
Từ ptpu ta có: \(n_{HCl}=x=\dfrac{0,4.2}{1}=0,8\left(mol\right)\)
=>\(m_{HCl}=n.M=0,8.\left(1+35,5\right)=29,2\left(g\right)\)
Lại có: mchất tham gia = mZn + mHCl = 26+29,2 =55,2(g)
msản phẩm = mH2 + mZnCl2 = 0,8 + 54,4 = 55,2 (g)
=>\(\dfrac{m_{chatthamgia}}{m_{sanpham}}=\dfrac{55,2}{55,2}=1\)