Khi đốt cháy hoàn toàn 2,2g hợp chất hữu cơ A thu được 8,1 g H2O. Ngoài ra không có chất nào khác. Biết rằng 0,84 lít hơi hợp chất A (DKTC) có khối lượng là 3,3g; TÌm cthh của hợp chất A
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


Đốt cháy A thu được sản phẩm chứa C, H, O
=> A chứa C, H và có thể có O
\(n_{CO_2}=\dfrac{4,4}{44}=0,1\left(mol\right)\Rightarrow n_C=0,1\left(mol\right)\)
\(n_{H_2O}=\dfrac{1,8}{18}=0,1\left(mol\right)\Rightarrow n_H=0,2\left(mol\right)\)
Xét mC + mH = 0,1.12 + 0,2.1 = 1,4 (g) < 2,2 (g)
=> A chứa C, H, O
\(n_O=\dfrac{2,2-1,4}{16}=0,05\left(mol\right)\)
Xét nC : nH : nO = 0,1 : 0,2 : 0,05 = 2 : 4 : 1
=> CTPT: (C2H4O)n
\(M_A=\dfrac{3,3}{\dfrac{0,84}{22,4}}=88\left(g/mol\right)\)
=> n = 2
=> CTPT: C4H8O2

Ta có:
\(n_X=\frac{0,84}{22,4}=0,0375\left(mol\right)\)
\(\Rightarrow M_A=\frac{3,3}{0,0375}=88\)
Đốt cháy 2,2 gam A thu được 4,4 gam CO2CO2 và 1,8 gam nước.
Nên A chứa C, H và O có thể có.
A có dạng \(C_xH_yO_z\Rightarrow12x+y+16z=88\)
\(C_xH_yO_z+\left(x+\frac{y}{4}+\frac{x}{2}\right)O_2\rightarrow xCO_2+\frac{y}{2}H_2O\)
\(n_A=\frac{2,2}{88}=0,025\left(mol\right)\)
\(n_{CO2}=\frac{4,4}{44}=0,1\left(mol\right)\)
\(n_{H2O}=\frac{1,8}{18}=0,1\left(mol\right)\)
\(x=\frac{n_{CO2}}{n_A}=\frac{0,1}{0,025}=4;y=\frac{2n_{H2O}}{n_A}=\frac{0,1.2}{0,025}=8\Rightarrow z=2\)
Vậy A là C4H8O2

\(n_{CO_2}=\dfrac{6,6}{44}=0,15\left(mol\right)\)
\(n_{H_2O}=\dfrac{3,6}{18}=0,2\left(mol\right)\)
Bảo toán C: nC(A) = 0,15 (mol)
Bảo toàn H: nH(A) = 0,2.2 = 0,4 (mol)
=> \(n_O=\dfrac{2,2-0,15.12-0,4.1}{16}=0\left(mol\right)\)
Xét nC : nH = 0,15 : 0,4 = 3:8
=> CTPT: (C3H8)n
Mà MA = 22.2 = 44(g/mol)
=> n = 1
=> CTPT: C3H8

Sửa đề : 1.4375
nCO2 = 2.2/44 = 0.05 (mol)
nH2O = 1.35/18 = 0.075 (mol)
mO = mY - mC - mH = 1.15 - 0.05*12 - 0.075*2 = 0.4(g)
nO = 0.4/16 = 0.025 (mol)
CT : CxHyOz
x : y : z = 0.05 : 0.15 : 0.025 = 2 : 6 : 1
CT nguyên : (C2H6O)n
MY = 1.4375*32 = 46 (g/mol)
=> 46n = 45
=> n = 1
Ct : C2H6O
Không biết đề có nhầm lẫn gì không nhưng sản phẩm có ở trên hết rồi ấy bạn ơiii
Sửa đề: \(1,5375\to 1,4375\)
\(m_{sản\ phẩm}= m_{CO_2} + m_{H_2O} = 2,2 + 1,35 = 3,55(gam)\\ n_{CO_2} = \dfrac{2,2}{44} = 0,05(mol)\\ n_{H_2O} = \dfrac{1,35}{18} = 0,075(mol)\\ n_{O_2} = \dfrac{2,2+1,35-1,15}{32} = 0,075(mol)\\ \)
Suy ra:
\(n_C = n_{CO_2} = 0,05(mol)\\ n_H = 2n_{H_2O} = 2.0,075 = 0,15(mol)\\ n_O = 2n_{CO_2} + n_{H_2O} -2n_{O_2} = 0,025\\ n_Y = \dfrac{1,15}{1,4375.32} = 0,025\)
Vậy :
Số nguyên tử C = \(\dfrac{n_C}{n_Y} = 2\)
Số nguyên tử H = \(\dfrac{n_H}{n_Y} = 6\)
Số nguyên tử O = \(\dfrac{n_O}{n_Y} = 1\)
Vậy CTPT của Y : C2H6O
\(C_2H_6O + 3O_2 \xrightarrow{t^o} 2CO_2 + 3H_2O\)

Đáp án C
Vì đốt cháy A thu được CO2 và H2O nên A chứa C, H, có thể có O.
Khi đó gọi công thức phân tử của A là CxHyOz
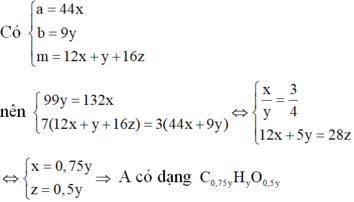
![]()
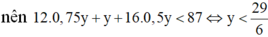
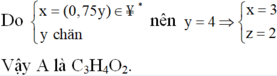
Nhận xét: Khi làm đến bước x : y = 3 :4 và kết hợp với quan sát 4 đáp án, ta có thể kết luận ngay A là C3H4O2.

Bảo toàn C: \(n_C=\dfrac{21,12}{44}=0,48\left(mol\right)\)
Bảo toàn H: \(n_H=2.\dfrac{8,64}{18}=0,96\left(mol\right)\)
Bảo toàn O: \(n_O=\dfrac{14,4-0,48.12-0,96}{16}=0,48\left(mol\right)\)
\(M_{hchc}=2,676.22,4=60\left(\dfrac{g}{mol}\right)\)
CTPT: CxHyOz
=> x : y : z = 0,48 : 0,96 : 0,48 = 1 : 2 : 1
=> (CH2O)n =60
=> n = 2
CTPT: C2H4O2
CTCT: CH3-COOH

a)
n CO2 = 6,6/44 = 0,15(mol) => n C = n CO2 = 0,15(mol)
n H2O = 5,4/18 = 0,3(mol) => n H = 2n H2O = 0,6(mol)
=> n O = (4,8 - 0,15.12 - 0,6)/16 = 0,15(mol)
Ta có :
n C : n H : n O = 0,15: 0,6 : 0,15 = 1 : 4 : 1
=> CTP của A là (CH4O)n
M A = (12 + 4 + 16)n = 3,2/(2,24/22,4) = 32
=> n = 1
Vậy CTPT của A là CH4O
b)
$2CH_3OH + 2Na \to 2CH_3ONa + H_2$
n CH3OH = n CO2 = 0,15(mol)
=> n H2 = 1/2 n CH3OH = 0,075(mol)
=> V H2 = 0,075.22,4 = 1,68(lít)

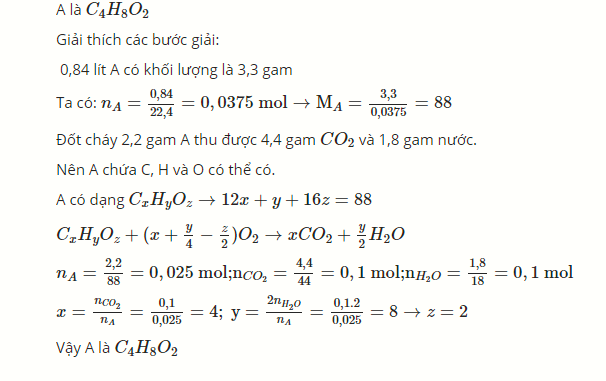
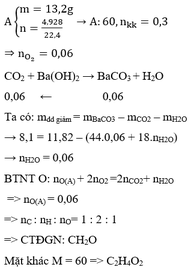


.Có nC = nCO2 = 0,1mol
nH = 2nH2O = 2.0,1 = 0,2 mol
mO = 2,2 - 0,1.12 - 0,2= 0,8=> nO= 0,05mol
=> CTDGN : C2H4O
2. Ta có nO2 =0,4/32 = 0,0125mol
=> nA = nO2 = 0,0125
=> MA = m/n = 1,1/0,0125=88
Ta có : (12.2 + 4 + 16) . n = 88 => n= 2
=> CT: C4H8O2