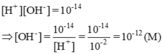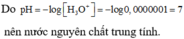12. Tính pH của một số dung dịch acid, base đơn bậc đơn giản. 13. Sự thuỷ phân muối và xác định pH môi trường của các dung dịch muối đó.
14. Dung dịch đệm là gì? Cấu trúc của dung dịch đệm? Tính pH của dung dịch đệm? Ứng dụng của dung dịch đệm.
15. Chất điện ly mạnh kém tan? Cho ví dụ. Cân bằng trong dung dịch chất điện ly kém tan? Độ tan? Tích số tan? Điều kiện hòa tan và tạo thành kết tủa của một chất điện ly kém tan AmBn(r)?
16. Áp suất hơi nước bão hòa là 17,5 mmH
giúp với máy ac ơi......