Cho 2 lít dung dịch hỗn hợp gồm: HCl 1M và H2SO4 0,5M phản ứng với 1 lít dung dịch hỗn hợp gồm: NaOH 3M và KOH 4M. Sau phản ứng hoàn toàn thu được dung dịch B. pH dung dịch B là:
A. 7 B. 1 C. 2 D. 13
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

a.Ta có n HCl = 1 . 0,25 = 0,25 mol
nH2SO4 = 0,5.0.25 = 0,125 mol
==> nH(X) = 0,25 + 0,125.2 = 0,5 mol
nH2 = 4,368/22,4 = 0,195 mol <=> nH= 0,195. 2 = 0,39 mol < 0,5 mol
Vậy sau phản ứng dung dịch B vẫn còn axit dư
b. Gọi số mol của Al và Mg lần lượt là x và y mol
Ta có phương trình 27x + 24y =3,87 (1)
Áp dụng định luật bảo toàn eletron ==> 3x + 2y = 0,195.2 (2)
Từ (1) , (2) ==> \(\left\{{}\begin{matrix}x=0,09\\y=0,06\end{matrix}\right.\)
mAl = 0,09 .27 = 2,43 gam , %mAl trong A = \(\dfrac{2,43}{3,87}\).100=62,8%
==> %mMg trong A = 100 - 62,8 = 37,2%

Đáp án A
Cho HCl 0,5M và H2SO4 0,25M vào 0,5 mol NaAlO2 và 0,5 mol NaOH thu được dung dịch X và 0,2 mol kết tủa Al(OH)3
Để cho lượng axit lớn nhất thì axit phải tham gia trung hòa hết NaOH, tạo kết tủa tới tối đa rồi sau đó hòa tan kết tủa tới khi còn 0,2 mol
→ n H + = 0 , 5 + 0 , 5 + ( 0 , 5 - 0 , 2 ) . 3 = 1 , 9 m o l → V = 1 , 9 0 , 5 + 0 , 25 . 2 = 1 , 9

Đáp án A
Cho HCl 0,5M và H2SO4 0,25M vào 0,5 mol NaAlO2 và 0,5 mol NaOH thu được dung dịch X và 0,2 mol kết tủa Al(OH)3
Để cho lượng axit lớn nhất thì axit phải tham gia trung hòa hết NaOH, tạo kết tủa tới tối đa rồi sau đó hòa tan kết tủa tới khi còn 0,2 mol
![]()
→ V = 1 , 9

Đáp án C
Phần 1: Tác dụng vói dung dịch H2SO4 loãng gồm Al và FexOy nên n H 2 = 3 2 n Al ⇒ n Al = 0 , 02
Phần 2: Thực hiện phản ứng nhiệt nhôm hoàn toàn và hỗn hợp B tác dụng với dung dịch NaOH dư có H2 nên B có Fe, A12O3 và Al dư. Có n Al du = 2 3 n H 2 ( NaOH ) = 0 , 004 .
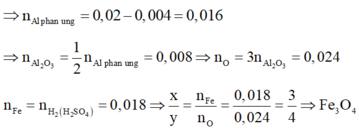

nHCl = 0,5.1,4 = 0,7 (mol) ; nH2SO4 = 0,5.0,5 = 0,25 (mol) => nSO42- = nH2SO4 = 0,25 (mol)
∑ nH+ = nHCl + 2nH2SO4 = 0,7 + 2.0,25 = 1,2 (mol)
nNaOH = 2V (mol) ; nBa(OH)2 = 4V (mol)
∑ nOH- = nNaOH + 2nBa(OH)2 = 2V + 2.4V = 10V (mol)
Các PTHH xảy ra:
H+ + OH- → H2O (1)
Ba2+ + SO42- → BaSO4↓ (2)
Khi cho Zn vào dd C thấy có khí H2 thoát ra => có 2 trường hợp có thể xảy ra. Zn có thể bị hòa tan bởi dung dịch axit hoặc bazo
nH2 = 3,36 : 22,4 = 0,15 (mol)
TH1: dd C có chứa H+ dư => phản ứng (1) OH- phản ứng hết
Zn + 2H+ → Zn2+ + H2↑ (3)
0,3 ← 0,15 (mol)
=> nH+ (1) = ∑ nH+ - nH+ dư = 1,2 – 0,3 = 0,9 (mol)
Theo (1): ∑nOH- = nH+ (1) = 0,9 = 10V => V = 0,09 (lít)
nBa(OH)2 = 4.0,09 = 0,36 => nBa2+ = nBa(OH)2 = 0,36 (mol) > nSO42-
Từ PTHH (2) => nBaSO4 = nSO42- = 0,25 (mol) => mBaSO4 = 0,25.233 = 58,25(g)
TH2: dd C có chứa OH- dư => phản ứng (1) H+ phản ứng hết
Zn + 2OH- → ZnO22- + H2↑ (4)
0,3 ← 0,15 (mol)
=> ∑ nOH- = nOH-(1) + nOH- (4) = 1,2 + 0,3 = 1,5 (mol)
=> 10V = 1,5
=> V = 0,15 (lít)
=> nBa(OH)2 = 0,15. 4 = 0,6 (mol)
=> nBa2+ = 0,6 (mol) > nSO42- = 0,25 (mol)
=> mBaSO4 = 0,25.233 = 58,25 (g)
14