Hoà tan 19,75 gam một muối hiđrocacbonat vào nước thu được dung dịch X. Cho X tác dụng với một lượng dung dịch H2SO4 10% vừa đủ, sau đó đem cô cạn dung dịch thì thu được 16,5 gam một muối sunfat trung hoà khan. Công thức phân tử của muối hiđrocacbonat là
A. Ba(HCO3)2
B. NaHCO3
C. Mg(HCO3)2
D. NH4HCO3



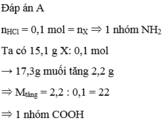


Đáp án là D. NH4HCO3