Cho 200ml dung dịch AlCl3 1,5M tác dụng với V lít dung dịch NaOH 0,5M; lượng kết tủa thu được là 15,6 gam. Giá trị lớn nhất của V là:
A. 1,2
B. 1,8
C. 2,4
D. 2
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Bài 1:
400ml dd E chứa \(\left\{{}\begin{matrix}AlCl_3:0,4x\left(mol\right)\\Al_2\left(SO_4\right)_3:0,4y\left(mol\right)\end{matrix}\right.\)
Xét TN2:
\(n_{BaSO_4}=\dfrac{33,552}{233}=0,144\left(mol\right)\)
=> \(n_{Al_2\left(SO_4\right)_3}=\dfrac{0,144}{3}=0,048\left(mol\right)\)
=> y = 0,12
Xét TN1:
\(n_{Al\left(OH\right)_3}=\dfrac{8,424}{78}=0,108\left(mol\right)\)
nNaOH = 0,612.1 = 0,612 (mol)
Do \(3.n_{Al\left(OH\right)_3}< n_{NaOH}\) => Kết tủa bị hòa tan 1 phần
PTHH: Al2(SO4)3 + 6NaOH --> 3Na2SO4 + 2Al(OH)3
0,048------>0,288------------------->0,096
AlCl3 + 3NaOH --> 3NaCl + Al(OH)3
0,4x--->1,2x------------------>0,4x
Al(OH)3 + NaOH --> NaAlO2 + 2H2O
(0,324-1,2x)<-(0,324-1,2x)
=> 0,096 + 0,4x - (0,324-1,2x) = 0,108
=> x = 0,21
=> \(\dfrac{x}{y}=\dfrac{0,21}{0,12}=\dfrac{7}{4}\)
Bài 3:
\(n_{Al_2\left(SO_4\right)_3}=\dfrac{200.1,71\%}{342}=0,01\left(mol\right)\)
\(n_{Al\left(OH\right)_3}=\dfrac{0,78}{78}=0,01\left(mol\right)\)
- Nếu kết tủa không bị hòa tan:
PTHH: 6NaOH + Al2(SO4)3 --> 3Na2SO4 + 2Al(OH)3
0,03<-------------------------------0,01
=> \(C_M=\dfrac{0,03}{0,2}=0,15M\)
- Nếu kết tủa bị hòa tan 1 phần
PTHH: 6NaOH + Al2(SO4)3 --> 3Na2SO4 + 2Al(OH)3
0,06<---0,01-------------------------->0,02
Al(OH)3 + NaOH --> NaAlO2 + 2H2O
0,01---->0,01
=> \(C_M=\dfrac{0,06+0,01}{0,2}=0,35M\)

Đáp án B
Số mol AlCl3 là nAlCl3= 0,1.1 = 0,1 (mol)
Số mol Al2O3 là nAl2O3= 2,55/102 = 0,025 (mol)
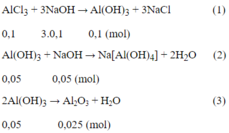
Theo pt (3) ta thấy số mol Al(OH)3 còn lại là 0,05 mol
Như vậy đã có: 0,1 - 0,05 = 0,05 mol Al(OH)3 đã bị hòa tan.
Từ (1) và (2) số mol NaOH = 3.0,1 + 0,05 = 0,35 (mol)
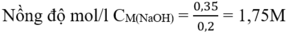

1.1. Al + NaOH + H2O ==> NaAlO2 + 3/2H2
nH2(1)=3,36/22,4=0.15(mol)
=> nAl(1)= nH2(1):3/2= 0.15:3/2= 0.1(mol)
2.Mg + 2HCl ==> MgCl2 + H2
3.2Al + 6HCl ==> 2AlCl3 + 3H2
4.Fe + 2HCl ==> FeCl2 + H2
=> \(n_{H_2\left(2,3,4\right)}=\) 10.08/22.4= 0.45(mol)
=> nH2(3)=0.1*3/2=0.15(mol)
MgCl2 + 2NaOH ==> Mg(OH)2 + 2NaCl
AlCl3 + 3NaOH ==> Al(OH)3 + 3NaCl
FeCl2 + 2NaOH ==> Fe(OH)2 + 2NaCl

\(n_{K_2SO_4}=0,25mol\)
\(n_{Na_2CO_3}=0,25mol\)
\(n_{Ba\left(NO_3\right)_2}=0,5Vmol\)
\(n_{BaCl_2}=Vmol\)
Ba2++SO42-\(\rightarrow\)BaSO4
Ba2++CO32-\(\rightarrow\)BaCO3
ta có: 0,25+0,25=0,5V+V giải ra V=\(\dfrac{1}{3}l\)
Các ion trong dd sau phản ứng:
K+=Na+=0,25mol suy ra nồng độ mol=0,25/(\(\dfrac{1}{3}+0,25\))=0,43M
NO3- 0,5/3mol suy ra nồng độ mol=0,5/3:(\(\dfrac{1}{3}+0,25\))=0,29M
Cl- 1/3mol suy ra nồng độ mol=1/3:(\(\dfrac{1}{3}+0,25\))=0,57M

1. HCl + NaOH => NaCl + H2O (1)
nNaOH = 0,05.1 = 0,05 (mol)
(1) => nHCl = nNaOH = 0,05 (mol)
Trong 100 ml dd X có 0,05 mol HCl
=> Trong 200 ml dd X có 0,1 mol HCl
VHCl = 0,1.22,4 = 2,24 (l)
2. MnO2 + 4HClđ=>MnCl2 + Cl2 +2H2O(2)
nMnO2 = \(\frac{34,8}{87}=0,4\left(mol\right)\)
(2) => nCl2 = nMnO2 = 0,4 (mol)
=> VCl2 = 0,4.22,4 = 8,96 (l)
3. Cl2 + 2NaBr => 2NaCl + Br2 (3)
Cl2 + 2NaI => 2NaCl + I2 (4)
nNaCl = \(\frac{23,4}{58,5}=0,4\left(mol\right)\)
(3),(4) => nhỗn hợp ban đầu = nNaCl = 0,4 (mol)
4. X + Cl2 => B
X + HCl => C
X + B => C
=> X : Fe

Tham khảo
Cho hỗn hợp X vào dung dịch HCl lấy dư:
PTHH: Al2O3 + 6HCl → 2AlCl3 + 3H2O
MgO + 2HCl → MgCl2 + H2O
Fe + 2HCl → FeCl2 + H2
Dung dịch Y gồm: AlCl3, MgCl2, FeCl2, HCl dư
Khí Z là H2
Chất rắn A là Cu
Cho A tác dụng với H2SO4 đặc nóng.
PTHH: Cu + 2H2SO4(đặc, nóng) → CuSO4 + SO2 + 2H2O
Khí B là SO2
Cho B vào nước vôi trong lấy dư
PTHH: SO2 + Ca(OH)2 → CaSO3 + H2O
Kết tủa D là CaSO3
Cho dung dịch NaOH vào Y tới khi kết tủa lớn nhất thì dừng lại.
PTHH: NaOH + HCl → NaCl + H2O
3NaOH + AlCl3 → Al(OH)3 + 3NaCl
2NaOH + MgCl2 → Mg(OH)2 + 2NaCl
2NaOH + FeCl2 → Fe(OH)2 + 2NaCl
Chất rắn E là: Al(OH)3, Mg(OH)2, Fe(OH)2
Nung E trong không khí
Chất rắn G là Al2O3, MgO, Fe2O3

Đáp án B
1-đúng, Cr bị thụ động.
2-sai, CrO3 là oxit axit.
3-đúng.
4-sai, Cr tác dụng với Cl2 tạo ra CrCl3.
5-đúng.
6-sai, Cr hoạt động mạnh hơn Fe

Đáp án B
1-đúng, Cr bị thụ động.
2-sai, CrO3 là oxit axit.
3-đúng.
4-sai, Cr tác dụng với Cl2 tạo ra CrCl3.
5-đúng.
6-sai, Cr hoạt động mạnh hơn Fe.
Đáp án D
Ta có: n A l C l 3 = 1,5.0,2 = 0,3 mol; n A l ( O H ) 3 = 15 , 6 78 = 0,2 mol
Thể tích NaOH lớn nhất khi kết tủa sinh ra cực đại, bị NaOH hòa tan 1 phần còn 15,6 (g).
Theo phương trình phản ứng, ta có: nNaOH = 0,9 + 0,1 = 1 mol
⇒VNaOH = 1/0,5 = 2 lít