Hỗn hợp khí A chứa 2 anken kế tiếp nhau trong dãy đồng đẳng. Tỉ khối của A đối với khí nitơ là 1,35.
1. Xác định công thức phân tử 2 anken.
2. Nếu hiđrat hoá một lượng hỗn hợp A (giả sử hiệu suất là 100%) thì được hỗn hợp ancol B, trong đó tỉ lệ về khối lượng giữa ancol bậc một và ancol bậc hai là 43 : 50.
Hãy cho biết tên và phần trăm về khối lượng của từng ancol trong hỗn hợp B.


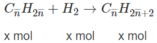
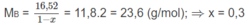
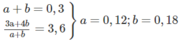


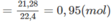
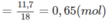
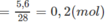
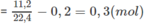


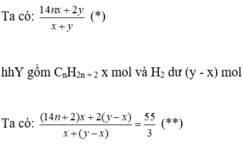

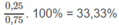
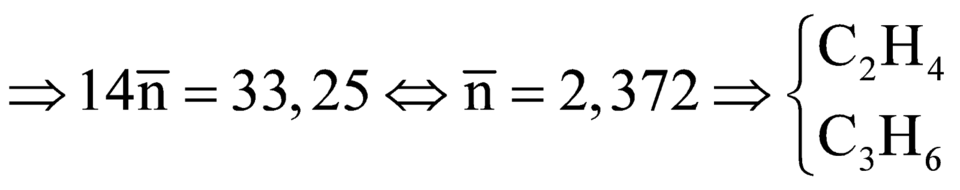
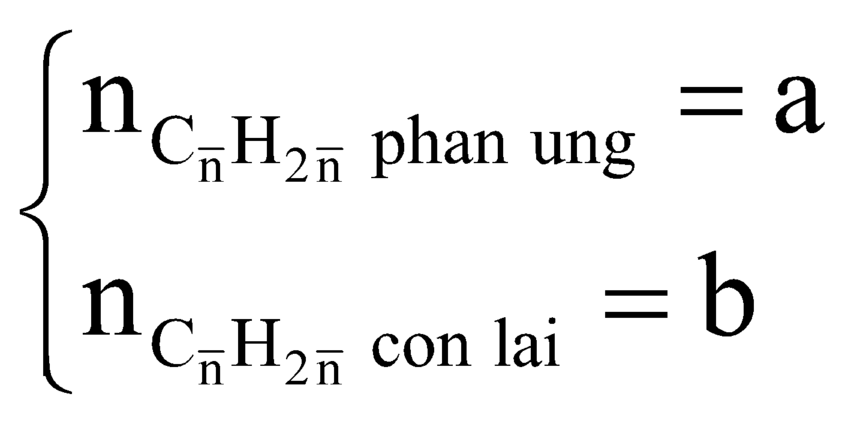


1. Hỗn hợp khí A chứa C n H 2 n và C n + 1 H 2 n + 2 với phân tử khối trung bình là: 1,35 x 28 = 37,8
⇒ C n H 2 n < 37,8 < C n + 1 H 2 n + 2
⇒ 14n < 37,8 < 14n + 14
1,70 < n < 2,70 ⇒ n = 2.
CTPT của 2 anken là C 2 H 4 và C 3 H 6 .
2. Giả sử trong 1 moi hỗn hợp A có x mol C 3 H 6 và (1 - x) mol C 2 H 4 :
42x + 28(1 - x) = 37,8 ⇒ x = 0,7
Như vậy, trong 1 mol hỗn hợp A có 0,7 mol C 3 H 6 và 0,3 mol C 2 H 4 .
Giả sử hiđrat hoá hoàn toàn 1 mol A :
C H 2 = C H 2 + H 2 O → C H 3 - C H 2 - O H
0,3 mol 0,3 mol
C H 3 - C H = C H 2 + H 2 O → C H 3 - C H 2 - C H 2 - O H
a mol a mol
Tỉ lệ khối lượng giữa ancol bậc I so với ancol bậc II :
Hỗn hợp B gồm 0,3 mol C H 3 - C H 2 - O H ; 0,2 mol C H 3 - C H 2 - C H 2 - O H và 0,5 mol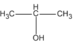 ; có khối lượng tổng cộng là 55,8 g.
; có khối lượng tổng cộng là 55,8 g.
% về khối lượng etanol (ancol etylic) là:
% về khối lượng của propan-l-ol (ancol propylic) là :
Propan-2-ol (ancol isopropylic) chiếm:
Riêng câu 2 cũng có thể lập luận như sau :
Phần trăm khối lượng của ancol bậc II (ancol isopropylic) :
Vậy phần trăm khối lượng của 2 ancol bậc I là 46,2%.
Nếu dùng 1 mol A (37,8 g) thì lượng H2O là 1 mol (18 g) và khối lượng hỗn hợp B là 37,8 + 18, = 55,8 (g), trong đó 0,3 mol C2H4 tạo ra 0,3 mol ancol etylic.
Phần trăm khối lượng của ancol etylic là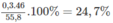
và của ancol propylic là: 46,2% - 24,7% = 21,5%.