Cho 23 gam hỗn hợp X gồm Al, Cu, Fe tác dụng với 400ml dung dịch CuSO4 1M đến khi phản ứng xong, thu được dung dịch Z và m gam hỗn hợp T gồm 2 kim loại. Cho Z tác dụng với dung dịch NaOH, thu được lượng kết tủa lớn nhất là 24,6 gam. Giá trị của m là:
A. 37,6
B. 27,7
C. 19,8
D. 42,1


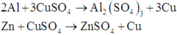



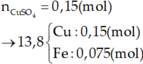
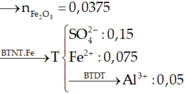
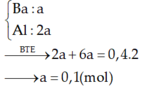
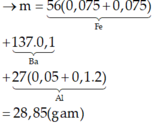




Đáp án A
Vì T gồm hai kim loại nên T chứa Cu và Fe dư. Khi đó Cu3+ phản ứng hết và dung dịch Z có Al3+ và có thể có Fe2+.
Theo định luật bảo toàn điện tích, ta có: