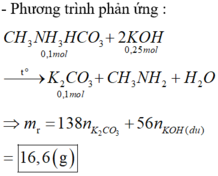
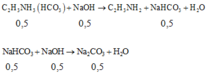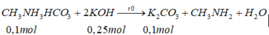X là hợp chất có công thức phân tử C 3 H 7 O 3 N . X phản ứng với dung dịch HCl hay dung dịch NaOH đều có khí không màu thoát ra. Cho 0,5 mol X phản ứng với 3 mol NaOH, sau phản ứng cô cạn dung dịch khối chất rắn thu được là
A. 133
B. 53
C. 142,5
D. 42,5