Hòa tan hoàn toàn a gam hỗn hợp Na, K, Ba, Al vào nước, thu được dung dịch T và 8,512 lít H2. Cho T phản ứng với 200 ml dung dịch H2SO4 1,25M và HCl 1M, thu được 24,86 gam kết tủa và dung dịch Z chỉ chứa các muối clorua và sufat trung hòa. Cô cạn Z, thu được 30,08 gam chất rắn khan. Phần trăm khối lượng Ba trong hỗn hợp đầu là
A. 49,19%.
B.60,04%.
C.58,64%.
D.48,15%.


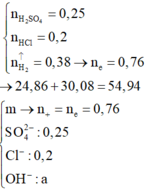
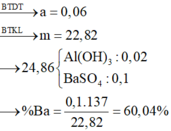
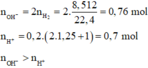
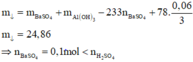
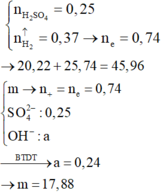
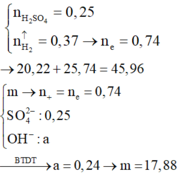
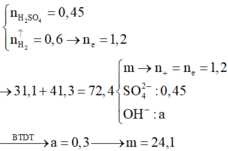
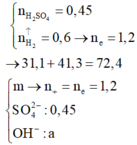
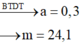



Đáp án B
Vì dung dịch Z chỉ chứa muối clorua và sunfat trung hòa nên H2SO4 và HCl phản ứng hết.
Bảo toàn electron có: nNa + nK + 2nBa + 3nAl = 2nH2 = 0,78 mol.
Có 24,86g + 30,08g gồm các thành phần sau Na+, K+, Ba2+, Al3+, SO42–: 0,25; Cl– : 0,2 mol; OH–.
Bảo toàn điện tích → nOH- = nNa+ + 2nBa2+ + 3nAl3+ - 2SO42- - nCl– = 0,76 - 2. 0,25 - 0,2 = 0,06 mol.
⇒ nAl(OH)3 = 1 3 .nOH– = 0,02 mol.
mkết tủa = mAl(OH)3 + mBaSO4 = 24,86 gam ⇒ nBaSO4 = 0,1 mol.
Do SO42– còn dư nên Ba2+ đi hết vào kết tủa: nBa = nBaSO4 = 0,1 mol.
→ mNa + mK + mBa + mAl = 24,86 + 30,08 - 0,25. 96 - 0,2.35,5 - 0,06. 17 = 22,82 gam.
⇒ %mBa = 0 , 1 . 137 22 , 82 .100% = 60,04%.