Hòa tan m gam hỗn hợp T gồm F e x O y , F e v à C u bằng dung dịch chứa 1,8 mol HCl và 0,3 mol H N O 3 , sau phản ứng thu được 5,824 lít NO(đktc, sản phẩm khử duy nhất) và dung dịch X chứa (m + 60,24) gam chất tan. Cho a gam Mg vào dung dịch X, kết thúc phản ứng thu được (m - 6,04) gam rắn và hỗn hợp Y gồm hai khí (trong đó có một khí hóa nâu trong không khí) có tỉ khối so với He bằng 4,7. Giá trị của a gần nhất với giá trị nào sau đây?
A. 21,0
B. 23,0
C. 22,0
D. 24,0


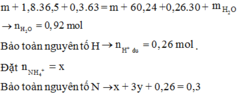
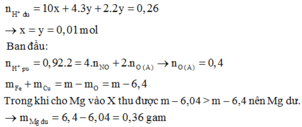
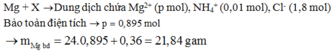


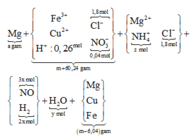
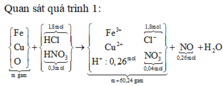
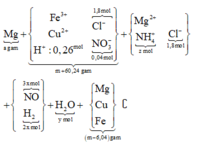
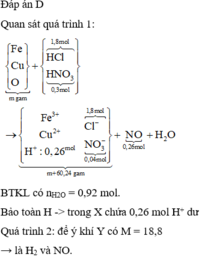

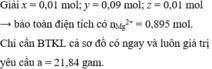
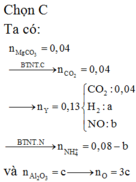


Đáp án C