Hòa tan hết 10,24 gam Cu bằng 200 ml dung dịch HNO3 3M được dung dịch X. Thêm 400 ml dung dịch NaOH 1M vào dung dịch X. Lọc bỏ kết tủa, cô cạn dung dịch rồi nung chất rắn đến khối lượng không đổi thu được 26,44 gam chất rắn. Số mol HNO3 đã phản ứng với Cu là
A. 0,56 mol.
B. 0,4 mol.
C. 0,58 mol.
D. 0,48 mol.


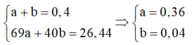



Chọn đáp án A
Giả sử toàn bộ Na → NaNO3 ⇒ nhiệt phân tạo thành NaNO2
⇒ mNaNO2 = 0,4 × 69 = 27,6 > 26,44 ⇒ Có NaOH dư.
+ Đặt nNaNO2 = a và nNaOHdư = b
⇒ Ta có hệ:
+ Nhận thấy nHNO3 = 0,6 mol nhưng nNO3– = 0,36 mol
⇒ nN bay ra theo khí = 0,6 – 0,36 = 0,24 mol.
+ Ta có nHNO3 pứ = nN/Cu(NO3)2 + nN bay ra theo khí = 2nCu + 0,24 = 0,56 mol
⇒ Chọn A