Cho mình hỏi liên kết cho nhận tương ứng với bao nhiêu hoá trị vậy ?
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


Trong các hợp chất cộng hoá trị thì cộng hoá trị của một nguyên tố được xác định bằng số liên kết cộng hoá trị của nguyên tử tương ứng trong phân tử.

a: tìm được 1 giá trị duy nhất tương ứng của s
b: Có thể tìm được 2 giá trị tương ứng của t
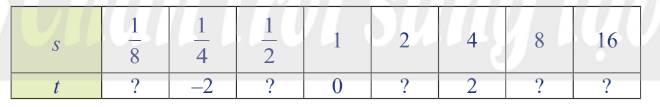
c:
| s | 1/8 | 1/4 | 1/2 | 1 | 2 | 4 | 8 | 16 |
| t | -3 | -2 | -1 | 0 | 1 | 2 | 3 | 4 |

Bạn có thể tham khảo cách làm các dạng bài tập viết công thức cấu tạo, từ đó rút ra cách viết đơn giản nhất cho mình. Mình nghĩ chắc cách viết nguyên tử dưới dạng mạch thẳng -> bẻ nguyên tử tạo thành các nhánh phụ ....... đó đơn giản lắm rồi!

Năng lượng tỏa ra của phản ứng:
(Tổng độ hụt khối sau - Tổng độ hụt khối trước).c2
\(=(\Delta m_{\alpha}+\Delta m_{n}-\Delta m_{T}-\Delta m_{D})c^2\)
\(=(W_{lk \alpha}-W_{lkT}-\Delta m_{D}.c^2)\)
\(=(7,0756.4-2,823.3-0,0024.931)\)
\(=...\)

Các nguyên tố thuộc nhóm VIIA gồm các nguyên tố : flo (F), clo (Cl), brom (Br), iot (I), atatin (At). Nguyên tử của chúng có 7 electron hoá trị.
Khi hai nguyên tử của cùng một nguyên tố thuộc nhóm này liên kết với nhau tạo thành phân tử thì mỗi nguyên tử góp 1 electron, tạo thành một cặp electron chung tức là một liên kết, vì mỗi nguyên tử chỉ thiếu electron để đạt được cấu hình 8 electron vững bền (giống như của khí hiếm đứng sau nó).
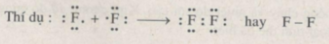


Liên kết cộng hóa trị, còn gọi là liên kết phân tử là một liên kết hóa học được hình thành bằng việc dùng chung một hay nhiều cặp electron giữa các nguyên tử. Những cặp electron này được gọi là cặp electron dùng chung, và sự cân bằng lực hút và lực đẩy giữa các nguyên tử trong khi chia sẻ các electron được gọi là liên kết cộng hóa trị.[1][cần nguồn tốt hơn] Với nhiều phân tử, việc dùng chung electron cho phép mỗi nguyên tử đạt được cấu hình electron bền vững. và 1 liên kết tương ứng với 1 hóa trị hoặc hơn tùy vào chất đó.
?? vậy là tương ứng với bao nhiêu hoá trị vậy bạn