Nung canxi cacbonat CacO3 ở nhiệt độ cao, ta đc canxi oxit CaO và khí Co2(ta nới CaCO3 bị nhiệt phân)
a)Tìm số mol CacO3 để điều chế được 5,6g CaO
b)với 25g CacO3 điều chế được bnhieu gam Cao? Bnhieu lít Co2(đktc)
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

a, CaCO3 --t0--> CaO + CO2
b, Ta có nCO2= 5,6/22,4=0,25 = nCaCO3
=> mCaCO3= 0,25.100=25 g
c, nCaO = nCO2=0,25
=> mCaO= 0,25.56=14 g

Đáp án
Vì khi nung ( C a C O 3 ) , khí C O 2 thoát ra nên khối lượng chất rắn thu được sau phản ứng giảm. Phương trình hóa học :
C a C O 3 → t ° C a O + C O 2

\(CaCO_3 \to CaO+CO_2\\ BTKL:\\ m_{CaCO_3}=m_{CaO}+m_{CO_2}\\ 150=m_{CaO}+66\\ \to m_{CaO}=84(g)\)

Khi nung đá vôi thì tạo ra lượng khí C O 2 đáng kể thoát ra ngoài nên làm khối lượng sản phẩm phản ứng giảm.

\(CaCO_3-^{t^o}\rightarrow CaO+CO_2\)
\(n_{CaO}=\dfrac{5,6}{56}=0,1\left(mol\right)\)
\(n_{CaCO_3}=n_{CaO}=0,1\left(mol\right)\\ \Rightarrow m_{CaCO_3}=0,1.100=10\left(g\right)\)
=> Chọn A

\(CaCO_3\rightarrow\left(t^o\right)CaO+CO_2\\ n_{CaCO_3}=\dfrac{200}{100}=2\left(mol\right)\\ n_{CaO}=\dfrac{100,8}{56}=1,8\left(mol\right)\\ V\text{ì}:\dfrac{2}{1}>\dfrac{1,8}{1}\Rightarrow CaCO_3d\text{ư}\\ n_{CaCO_3\left(p.\text{ứ}\right)}=n_{CaO}=1,8\left(mol\right)\\ m_{CaCO_3\left(d\text{ư}\right)}=200-1,8.100=20\left(g\right)\)

PTHH: \(CaCO_3\overset{t^o}{--->}CaO+CO_2\)
Áp dụng định luật bảo toàn khối lượng, ta được:
\(m_{CaCO_3}=m_{CaO}+m_{CO_2}=560+440=1000\left(g\right)=1\left(kg\right)\)
Vậy khối lượng CaCO3 đã dùng là 1 kg

Phương trình hóa học CaCO3 → CaO + CO2.
a) nCaO = 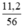 = 0,2 mol.
= 0,2 mol.
Theo PTHH thì nCaCO3 = nCaO = 0,2 (mol)
b) nCaO = 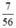 = 0,125 (mol)
= 0,125 (mol)
Theo PTHH thì nCaCO3 = nCaO = 0,125 (mol)
mCaCO3 = M.n = 100.0,125 = 12,5 (g)
c) Theo PTHH thì nCO2 = nCaCO3 = 3,5 (mol)
VCO2 = 22,4.n = 22,4.3,5 = 78,4 (lít)
d) nCO2 = 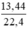 = 0,6 (mol)
= 0,6 (mol)
Theo PTHH nCaO = nCaCO3 = nCO2 = 0,6 (mol)
mCaCO3 = n.M = 0,6.100 = 60 (g)
mCaO = n.M = 0,6.56 = 33,6 (g)

\(n_{CaO}=\dfrac{m}{M}=0,2\left(mol\right)\)
\(PTHH:CaCO_3\rightarrow CaO+CO_2\)
.................0,2............0,2......0,2..........
a, \(m_{CaCO_3}=M.n=20\left(g\right)\)
b, \(V_{CO_2}=n.22,4=4,48\left(l\right)\)
Vậy ...
nCaO = 5,6 : 56 =0,1(mol)
PTHH : CaCO3 -t--> CaO +CO2
0,1(mol)<---------0,1
b ) nCaCO3= 25:100=0,25(mol)
theo pt trên nCaO = nCO2 = nCaCO3=0,25(mol)
=> mCaO = 0,25.56 =14(g)
=> V CO2 = 0,25 . 22,4 = 5,6 (L)
a) PTHH: CaCO3 \(\underrightarrow{t^o}\) CaO + CO2 (1)
1 1 1
0,1 0,1 0,1
nCaO = \(\dfrac{m}{M}\) = \(\dfrac{5,6}{56}\) = 0,1 (mol)
Từ (1) ⇒ 0,1 mol CaO ................... 0,1 mol CaCO3
Vậy cần 0,1 mol CaCO3 để điều chế được 5,6g CaO.
b) nCaCO3 = \(\dfrac{m}{M}\) = \(\dfrac{25}{100}\) = 0,25 (mol)
Từ (1) ⇒ 0,25 mol CaCO3 ................... 0,25 mol CaO
mCaO = n.M = 0,25 . 56 = 14 (g)
Từ (1) ⇒ 0,25 mol CaCO3 ................... 0,25 mol CO2
mCO2 = n.M = 0,25 . 44 = 11 (g)
VCO2 = 22,4 . m = 22,4 . 11 = 246,4 (l)