Chia m(g) hỗn hợp Fe , FeO, Fe3O4,Fe2O3 thành hai phần bằng nhau. Phần 1 : tác dụng vừa đủ vs 350ml dd H2SO4 loãng 1M giải phóng 3,36 lít khí H2 (đktc). Phần 2 tác dụng với dung dịch H2SO4 đặc, nóng, dư thu được 5,6 lít khí SO2 (đktc). Tính phần trăm khối lượng của Fe trong hỗn hợp.
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


\(\text{Mỗi phần,gọi :} n_{Al} = a ; n_{Fe} = b ; n_{Cu} = c\\ \Rightarrow 27a + 56b + 64c = \dfrac{35,8}{2} = 17,9(1)\\ \text{Phần 1 : Al,Fe không phản ứng với axit đặc nguội}\\ Cu + 2H_2SO_4 \to CuSO_4 + SO_2 + H_2O\\ n_{Cu} = c = n_{SO_2} = \dfrac{3,36}{22,4} = 0,15(2)\\ \text{Phần 2 : Cu không phản ứng với axit loãng}\\ 2Al + 3H_2SO_4 \to Al_2(SO_4)_3 + 3H_2\\ Fe + H_2SO_4 \to FeSO_4 + H_2\\ n_{H_2} = 1,5a + b = \dfrac{5,6}{22,4} = 0,25(3)\\ (1)(2)(3) \Rightarrow a = b = 0,1 ; c = 0,15\)
Suy ra :
\(m_{Al} = 0,1.2.27 = 5,4(gam)\\ m_{Fe} = 0,1.2.56 = 11,2(gam)\\ m_{Cu} = 0,15.64.2 = 19,2(gam)\)

Gọi \(\left\{{}\begin{matrix}n_{Cu}=x\left(mol\right)\\n_{Fe}=y\left(mol\right)\end{matrix}\right.\)
Phần 1:
\(n_{H_2}=\dfrac{4,48}{22,4}=0,2mol\)
\(Fe+H_2SO_{4l}\rightarrow FeSO_4+H_2\)
0,2 0,2
\(\Rightarrow n_{Fe}=0,2mol\Rightarrow m_{Fe}=0,2\cdot56=11,2g\)
Phần 2:
\(n_{SO_2}=\dfrac{8,96}{22,4}=0,4mol\)
\(BTe:2n_{Cu}+3n_{Fe}=2n_{SO_2}=0,8\)
\(\Rightarrow n_{Cu}=\dfrac{0,8-3\cdot0,2}{2}=0,1mol\)
\(\Rightarrow m_{Cu}=0,1\cdot64=6,4g\)
Vậy \(m_X=m_{Cu}+m_{Fe}=6,4+11,2=17,6g\)

Giải thích:
Chất rắn Y tác dụng với NaOH sinh ra H2 => Al dư => Chất rắn Y gồm: Al dư, Al2O3, Fe
nAl dư = nH2(P2)/1,5 = 0,0375/1,5 = 0,025 mol
nH2(P1) = nFe + 1,5nAl => nFe = 0,1375 – 1,5.0,025 = 0,1 mol
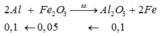
m(1 phần) = mAl ban đầu + mFe2O3 = 27(0,1+0,025) + 160.0,05 = 11,375 gam
=> m = 22,75 gam
Đáp án C

Chọn A
2 A l + F e 2 O 3 → A l 2 O 3 + 2 F e
Theo bài ra Y gồm: Fe, A l 2 O 3 và Al dư, giả sử với số mol lần lượt ở mỗi phần là x, y và z (mol). Theo PTHH → x = 2y (1)
Phần 1: bảo toàn e: 2x + 3z = 0,1375.2 = 0,275 (2)
Phần 2: bảo toàn e: 3z = 0,0375.2 = 0,075 (3)
Từ (1); (2); (3) có x = 0,1; y = 0,05; z = 0,025.
m = m Y = 2.(0,1.56 + 0,05.102 + 0,025.27) = 22,75 gam.


1/2m hỗn hợp= 39,2
m muối tăng= mSO4-mCl
do nso4(2-)=1/2ncl-(bảo toàn điện tích hoặc có thể viết pt ra là thấy)
83,95-77,7=96.1/2.ncl-35,5ncl
ncl bị thay thế là 0,5
có ở phần 77,7. có btkluong 39,2+36,5.2.a=77.7+18a(a là n h20)
a=0,7 ----- tổng ncl = 1,4
n kloai là 77,7-1,4.35.5=28 ----- nfeo là x fe2o3 y (ở nửa phần) có 56x+112y=28......72x+160y=39,2
x=0,1 y=0,2
%feo=18,36...... fe203=81,64%
b, ncl còn lại=nhcl=1,4-0,5=0,9
nso4=1/2ncl=0.25=nh2so4
CM=(0,25+0,9)/0,5=2,3