Nung a gam KClO3 và b gam KMnO4 thu được cùng một lượng O2. Tính tỉ lệ a/b
Câu 8. Lấy cùng một lượng KClO3 và KMnO4 để điều chế khí O2. Chất nào cho nhiều khí O2 hơn.
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Giả sử cần điều chế 3,36lit O 2 tương đương với 0,15 mol O 2
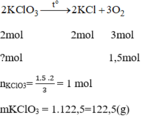
Số tiền mua 122,5g để điều chế 1,5mol O 2 :
0,1225.96000 = 11760 (đồng)
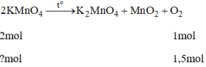
n K M n O 4 = 1,5 . 2 =3 mol
n K M n O 4 = 3.158 = 474 (g)
Số tiền mua 474g để điều chế 1,5 mol O 2 :
0,474.30000 = 14220(đồng)
Vậy để điều chế cùng 1 thể tích khí O 2 thì dùng K C l O 3 để điều chế kinh tế hơn mặc dù giá tiền cao mua 1 kg K C l O 3 cao hơn nhưng thể tích khí O 2 sinh ra nhiều hơn.

Giả sử ta lấy cùng một khối lượng là a g
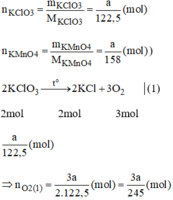
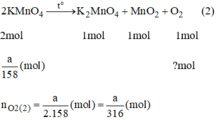
Vậy 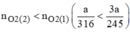 nên khi nhiệt phân cùng 1 lượng chất cho nhiều oxi hơn là
K
C
l
O
3
nên khi nhiệt phân cùng 1 lượng chất cho nhiều oxi hơn là
K
C
l
O
3

a. Phương pháp: đẩy nước vì oxi ít tan trong nước, đẩy không khí vì oxi nặng hơn không khí
b.Giả sử có 1 mol O2
\(2KMnO_4\rightarrow\left(t^o\right)K_2MnO_4+MnO_2+O_2\)
2 1 ( mol )
\(m_{KMnO_4}=2.158=316g\)
\(2KClO_3\rightarrow\left(t^o,MnO_2\right)2KCl+3O_2\)
2/3 1 ( mol )
\(m_{KClO_3}=\dfrac{2}{3}.122,5=\dfrac{245}{3}g\)
\(\dfrac{a}{b}=\dfrac{m_{KMnO_4}}{m_{KClO_3}}=316:\dfrac{245}{3}=\dfrac{948}{245}\)
a ) pp đẩy kk và đẩy nước
nKMnO4 = a / 158 (MOL)
nKClO3 = b / 122,5 (MOL)
b) gọi số mol O2 là x
pthh : 2KMnO4 -t--> K2MnO4 + MnO2 + O2
2x ---------------------------------> x (mol)
2KClO3 -t--> 2KCl+ 3O2
2/3x -----------> x(mol)
=> mKMnO4 = 2x . 158 = 316 x (g)
=> mKClO3 = 2/3 x . 122,5 = 81,67 x (g)
=> a/b = 316x/81,67x = 316 / 81,67

Bài 4. 2\(KMnO_4\) ---> \(K_2MnO_4\) + \(MnO_2\) + \(O_2\) (Lập và cân bằng phương trình)
0,6 mol 0,3 mol 0,3 mol 0,3 mol
a. + Số mol của \(O_2\)
\(n_{O_2}\) = \(\dfrac{V}{22,4}\) = \(\dfrac{6,72}{22,4}\) = 0,3 (mol)
+ Khối lượng của \(KMnO_4\) (thuốc tím) cần dùng:
\(m_{KMnO_4}\) = n . M = 0,6 . 158 = 94,8 (g)
b. 2\(KClO_3\) ---> 2\(KCl\) + 3\(O_2\) (Lập và cân bằng phương trình)
0,2 mol 0,2 mol 0,3 mol
Số g \(KClO_3\) dùng để điều chế:
\(m_{KClO_3}\) = n . M = 0,2 . 122,5 = 24,5 (g)
c. 2Cu + \(O_2\) ---> 2\(CuO\) (Lập và cân bằng phương trình)
0,6 mol 0,3 mol 0,6 mol
Số g của CuO sau phản ứng thu được:
\(m_{CuO}\) = n . M = 0,6 . 80 = 48 (g)
________________________________________
Bài 4 trước nha bạn, có gì sai thì nhắn mình :))
Bài 5. CuO + \(H_2\) ---> Cu + \(H_2O\) (Lập và cân bằng phương trình)
0,2 mol 0,2 mol 0,2 mol 0,2 mol
a. + Số mol của CuO:
\(n_{CuO}\) = \(\dfrac{m}{M}\) = \(\dfrac{16}{80}\) = 0,2 (mol)
+ Thể tích của \(H_2\)
\(V_{H_2}\) = n . 22,4 = 0,2 . 22,4 = 4,48 (lít)
b. Khối lượng Cu sau phản ứng:
\(m_{Cu}\) = n . M = 0,2 . 64 = 12,8 (g)
______________________________
Bài 5 nha, sai thì nhắn mình :))

PTHH :
\(2KClO_3\underrightarrow{t^o}2KCl+3O_2\)
1/3 0,5
\(2MnO_4\underrightarrow{t^o}K_2MnO_4+MnO_2+O_2\uparrow\)
1 0,5
Vậy khi điều chế cùng lượng O2 ta dùng KClO3 lợi hơn vì với 1 mol KClO3 sẽ cho ra 1,5 mol O2 còn KMnO4 chỉ cho ra 0,5 mol O2
\(n_{O_2}=\dfrac{11,2}{22,4}=0,5\left(mol\right)\)
\(m_{KClO_3}=122,5.\dfrac{1}{3}=\dfrac{245}{6}\approx40,8\left(g\right)\)
\(m_{KMnO_4}=158.1=158\left(g\right)\)

Có sự thay đổi số mol hỗn hợp khí xảy ra trong các phản ứng đốt cháy, hoặc đôi khi không thay đổi.
C/S + O2 → CO2/ SO2 (1)
2Al +3/2O2 → Al2O3 (2)
C, S hay A1, chúng là các chất rắn được đem đốt cháy với oxi hoặc một hỗn hợp khí chứa oxi,… và sau phản ứng người ta thu được một khí/hỗn hợp khí mới,…
Trong nhiều trường hợp, ta cần so sánh số mol hỗn hợp khí mới và cũ, như trong tình huống (1), hai giá trị này bằng nhau, tình huống (2) thì khác, khi có oxit tạo thành, tổng số mol khí sẽ giảm.
Với bài tập này, phản ứng của cacbon với oxi xảy ra và số mol hỗn hợp khí không thay đổi, đó chỉ là một sự thay thế như tăng giảm khối lượng vậy, O2 trở thành CO2 theo tỉ lệ 1:1 → nZ = nT
Bảo toàn nguyên tố C: nC/T = nCO2/T = 0,528/12 =0,044
→nT = 0,044/22,92% = 0,192 = nZ → nO2 trộn = 0,192/4 =0,048
→m = mY + mO2 = 0,894/8,132% + 32.0,048 = 12,5296
Chọn đáp án C

a)
\(2KMnO_4\xrightarrow[]{t^o}K_2MnO_4+MnO_2+O_2\) (1)
\(2KClO_3\xrightarrow[]{t^o}2KCl+3O_2\) (2)
\(n_{KCl}=\dfrac{0,894}{74,5}=0,012\left(mol\right);m_B=\dfrac{0,894}{8,132\%}=11\left(g\right)\)
Gọi \(n_{O_2\left(sinh.ra\right)}=a\left(mol\right)\Rightarrow n_{kk}=3a\left(mol\right)\)
\(\Rightarrow\left\{{}\begin{matrix}n_{N_2}=3a.80\%=2,4a\left(mol\right)\\n_{O_2}=a+\left(3a-2,4a\right)=1,6a\left(mol\right)\end{matrix}\right.\)
\(n_C=\dfrac{0,528}{12}=0,044\left(mol\right)\)
\(C+O_2\xrightarrow[]{t^o}CO_2\) (3)
Vì hỗn hợp D gồm 3 khí và O2 chiếm 17,083%
\(\Rightarrow D:CO_2,O_{2\left(d\text{ư}\right)},N_2\)
BTNT C: \(n_{CO_2}=n_C=0,044\left(mol\right)\)
BTNT O: \(n_{O_2\left(d\text{ư}\right)}=n_{O_2\left(b\text{đ}\right)}-n_{CO_2}=1,6a-0,044\left(mol\right)\)
\(\Rightarrow\%V_{O_2}=\%n_{O_2}=\dfrac{1,6a-0,044}{1,6a-0,044+0,044+2,4a}.100\%=17,083\%\)
\(\Leftrightarrow a=0,048\left(mol\right)\left(TM\right)\)
ĐLBTKL: \(m_A=m_B+m_{O_2}=11+0,048.32=12,536\left(g\right)\)
Theo PT (2): \(n_{KClO_3}=n_{KCl}=0,012\left(mol\right)\)
\(\Rightarrow\left\{{}\begin{matrix}\%m_{KClO_3}=\dfrac{0,012.122,5}{12,536}.100\%=11,63\%\\\%m_{KMnO_4}=100\%-11,63\%=88,37\%\end{matrix}\right.\)
b) Theo PT (2): \(n_{O_2}=\dfrac{1}{2}n_{KMnO_4\left(p\text{ư}\right)}+\dfrac{3}{2}n_{KClO_3}\)
\(\Rightarrow n_{KMnO_4\left(p\text{ư}\right)}=2.\left(0,048-\dfrac{3}{2}.0,012\right)=0,06\left(mol\right)\)
\(n_{KMnO_4\left(b\text{đ}\right)}=\dfrac{12,536-0,012.122,5}{158}=0,07\left(mol\right)\)
\(\Rightarrow n_{KMnO_4\left(d\text{ư}\right)}=0,07-0,06=0,01\left(mol\right)\)
\(n_{KCl}=\dfrac{74,5}{74,5}+0,012=1,012\left(mol\right)\)
Theo PT (1): \(n_{K_2MnO_4}=n_{MnO_2}=\dfrac{1}{2}.n_{KMnO_4\left(p\text{ư}\right)}=0,03\left(mol\right)\)
PTHH:
\(2KMnO_4+10KCl+8H_2SO_4\rightarrow6K_2SO_4+2MnSO_4+5Cl_2+8H_2O\) (4)
\(K_2MnO_4+4KCl+4H_2SO_4\rightarrow3K_2SO_4+MnSO_4+2Cl_2+4H_2O\) (5)
\(MnO_2+2KCl+2H_2SO_4\rightarrow MnSO_4+K_2SO_4+Cl_2+2H_2O\) (6)
\(2KCl+H_2SO_4\xrightarrow[]{t^o}K_2SO_4+2HCl\) (7)
Theo PT (4), (5), (6): \(n_{KCl\left(p\text{ư}\right)}=5n_{KMnO_4\left(d\text{ư}\right)}+4n_{K_2MnO_4}+2n_{MnO_2}=0,23\left(mol\right)< 1,012\left(mol\right)=n_{KCl\left(b\text{đ}\right)}\)
`=> KCl` dư
Theo PT (4), (5), (6): \(n_{Cl_2}=\dfrac{1}{2}.n_{KCl\left(p\text{ư}\right)}=0,115\left(mol\right)\)
\(\Rightarrow V_{kh\text{í}}=V_{Cl_2}=0,115.22,4=2,576\left(l\right)\)
Này là thành viên mới ha =))
là s