Câu 5: 2,24 lít hỗn hợp khí X gồm H2 và C2H4 có tỉ khối so với He là 2,125. Dẫn X qua Ni nung nóng đến khi phản ứng xảy ra hoàn
toàn, thu được hỗn hợp khí Y. Tính thể tích mỗi khí trong hỗn hợp Y?
Câu 6: Hỗn hợp 4,48 lít khí A gồm H2 và C2H4. Dẫn A qua Ni nung nóng đến khi phản ứng xảy ra hoàn toàn thu được hỗn hợp khí
Y có thể tích là 3,36 lít chỉ gồm các hidrocacbon
a) Tính thể tích mỗi khí trong hỗn hợp ban đầu?
b) Hỗn hợp Y có thể làm mất màu tối đa bao nhiêu mol Br2?
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án C
Hướng dẫn Ta có : M - X = 4. 3,75 = 15
C 2 H 4 28 13 \ / 15 / \ H 2 2 13
→ n C 2 H 4 n H 2 = 1 1
Vậy hiệu suất tính theo anken hoặc H2 củng được
Giả sử: nX = 1mol → mX = 15. 1 = 15 g = mY
Mà M - Y = 5. 4 = 20 → nY = 15/20 = 0,75 mol → nH2 pư = 1 – 0,75 = 0,25 mol
→ H = 0 , 25 0 , 5 .100% = 50%

Đáp án C
Hướng dẫn
Ta có : M - X = 4. 3,75 = 15
C 2 H 4 28 13 \ / 15 / \ H 2 2 13
→ n C 2 H n H 2 = 1 1
Vậy hiệu suất tính theo anken hoặc H2 củng được
Giả sử: nX = 1mol à mX = 15. 1 = 15 g = mY
Mà M - Y = 5. 4 = 20 à nY = 15/20 = 0,75 mol à nH2 pư= 1 – 0,75 = 0,25 mol
à H = 0 , 25 0 , 5 .100% = 50%

Đáp án D
hhX gồm H2 và C2H4 có dX/He = 3,75.
Dẫn X qua Ni, to → hhY có dY/He = 5.
• Đặt nH2 = x mol; nC2H4 = y mol.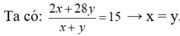
Đặt nH2 = 1 mol; nC2H4 = 1 mol.
Giả sử có x mol C2H6 tạo thành → hhY gồm C2H6 x mol; H2 (1 - x) mol và C2H4 (1 - x) mol.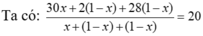
→ x = 0,5 → H = 50%

Đáp án D
MX = 15. Áp dụng qui tắc đường chéo : nC2H4 : nH2 = 1 : 1. Giả sử số mol mỗi chất trong X là 1
C2H4 + H2 ->C2H6
, x -> x -> x
=> nY = 2 – x mol
Bảo toàn khối lượng : mX = mY => 2 + 28 = 4.5.(2 – x)
=> x = 0,5 mol => H% = 50%

Giả sử nX =1
Có nH2 + nC2H4 = nX = 1
2nH2 + 28nC2H4 = mX = 3,75.4 = 15
⇒ nH2 = nC2H4 = 0,5
Đặt nC2H4 phản ứng = a ⇒ nH2 phản ứng = a.
⇒ nY = nX – nH2 phản ứng = 1 – a
MY = 5.4 =20
mY = mX =15 ⇒ nY = 15 : 20 =0,75 ⇒ a = 1- 0,75 = 0,25
⇒ H = 25%
Đáp án B.

Đáp án C
Hướng dẫn
Áp dụng sơ đồ đường chéo ta có :
n H 2 n C 2 H 4 = 28 - 15 15 - 2 = 1 1 Þ Có thể tính hiệu suất phản ứng theo H2 hoặc theo C2H4
Phương trình phản ứng :
H2 + C2H4 ![]() C2H6
C2H6
Áp dụng định luật bảo toàn khối lượng ta có :
mX = mY <=> nX. M - X = nY. M - Y <=> n X n Y = M - Y M _ X = 5 . 4 3 , 75 . 4 = 4 3
Chọn nX = 4 mol => n H 2 = n C 2 H 4 = 2 mol ; n H 2 ( p o ) . . = n X - n Y = 1 mol
=> Hiệu suất phản ứng : H = 1 2 .100% = 50%

n1 là số mol hỗn hợp khí ban đầu, n2 là số mol hỗn hợp khí sau phản ứng.

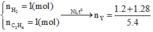



5.
\(n_X=\dfrac{2,24}{22,4}=0,1mol\\ M_X=2,125.4=8,5g\cdot mol^{^{ }-1}\\ n_{H_2}=a;n_{C_2H_4}=b\\ a+b=0,1\\ 2a+28b=8,5.0,1=0,85\\ a=0,075;b=0,025\\ H_2+C_2H_4-^{^{ }Ni,t^{^{ }0}}->C_2H_6\\ V_{C_2H_6}=0,025.22,4=0,56L;V_{H_2dư}=22,4\left(0,075-0,025\right)=1,12L\)
6.
Thu được Y chỉ gồm hydrocarbon nên khí hydrogen phản ứng hết.
\(n_A=\dfrac{4,48}{22,4}=0,2mol\\ n_Y=\dfrac{3,36}{22,4}=0,15mol\\ \Delta n_{hh}=n_{H_2\left(pư\right)}=0,05\left(mol\right)\\ n_{C_2H_4}=0,15\left(mol\right)\\ a.\%V_{H_2}=\dfrac{0,05}{0,2}=25\%\\ \%V_{C_2H_4}=75\%\\ b.BTLK\pi:0,15=0,05+n_{Br_2}\\ n_{Br_2}=0,1mol\)