A là hỗn hợp gồm: Ba, Al, Mg. Lấy m gam A cho tác dụng với nước tới khi hết phản ứng thấy thoát ra 3,36 lit H2 (đktc). Lấy m gam A cho vào dung dịch xút dư tới khi hết phản ứng thấy thoát ra 6,72 lít H2 (đktc). Lấy m gam A hoà tan bằng một lượng vừa đủ dung dịch axit HCl thì thu được một dung dịch và 8,96 lit H2 (đktc). Hãy tính m gam và thành phần % theo khối lượng của mỗi kim loại trong hỗn hợp.
Mong mọi người giúp đỡ


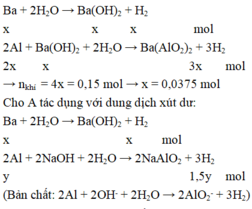

 ZnSO4 + H2
ZnSO4 + H2



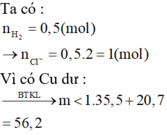
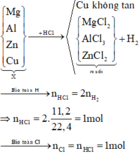
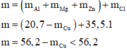

đáp án của bài theo quận hơi kì đó là :m=24,65g
mBa=19,55g
mAl=2,7g
mMg=2,4g
trong khi em ra mHH:= 12,2625g %mBa:=42% %mAl=38,5% %mMg=19,5%
mong mọi người giúp ạ
có khi đáp án của bài sai đấy