Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

3.
nHgO = 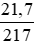
Phương trình hóa học của phản ứng khử HgO:
HgO + H2 → Hg + H2O
nHg = 0,1 mol.
mHg = 0,1 .201 = 20,1g.
nH2 = 0,1 mol.
VH2 = 0,1 .22,4 =2,24l.
1.
Phương trình phản ứng:
Fe3O4 + 4H2 → 4H2O + 3Fe
HgO + H2 → H2O + Hg
PbO + H2 → H2O + Pb

Câu 1 :
\(a.\) \(Fe_2O_3+3H_2\underrightarrow{^{^{t^0}}}2Fe+3H_2O\)
\(b.P_2O_5+3H_2O\rightarrow2H_3PO_4\)
\(c.Mg+2HCl\rightarrow MgCl_2+H_2\)
\(d.Na+H_2O\rightarrow NaOH+\dfrac{1}{2}H_2\)
\(e.CaO+H_2O\rightarrow Ca\left(OH\right)_2\)
\(f.Fe_3O_4+4H_2\underrightarrow{^{^{t^0}}}3Fe+4H_2O\)

a)\(CH_4+2O_2\underrightarrow{t^o}CO_2+2H_2O\)
\(C+O_2\underrightarrow{t^o}CO_2\)
\(S+O_2\underrightarrow{t^o}SO_2\)
\(4Al+3O_2\underrightarrow{t^o}2Al_2O_3\)
\(3Fe+2O_2\underrightarrow{t^o}Fe_3O_4\)
b)\(Fe_2O_3+3H_2\rightarrow2Fe+3H_2O\)
\(HgO+H_2\rightarrow Hg+H_2O\)
\(PbO+H_2\rightarrow Pb+H_2O\)
c)\(2Na+2H_2O\rightarrow2NaOH+H_2\)
\(CaO+H_2O\rightarrow Ca\left(OH\right)_2\)
\(Na_2O+H_2O\rightarrow2NaOH\)
\(SO_2+H_2O\rightarrow H_2SO_3\)
\(P_2O_5+3H_2O\rightarrow2H_3PO_4\)

a.\(CH_4+2O_2\rightarrow\left(t^o\right)CO_2+2H_2O\)
\(C+O_2\rightarrow\left(t^o\right)CO_2\)
\(S+O_2\rightarrow\left(t^o\right)SO_2\)
\(4Al+3O_2\rightarrow\left(t^o\right)2Al_2O_3\)
\(3Fe+2O_2\rightarrow\left(t^o\right)Fe_3O_4\)
b.\(Fe_2O_3+3H_2\rightarrow\left(t^o\right)2Fe+3H_2O\)
\(HgO+H_2\rightarrow\left(t^o\right)Hg+H_2O\)
\(PbO+H_2\rightarrow\left(t^o\right)Pb+H_2O\)
c.\(2Na+2H_2O\rightarrow2NaOH+H_2\)
\(Na_2O+H_2O\rightarrow2NaOH\)
\(SO_2+H_2O⇌H_2SO_3\)
\(P_2O_5+3H_2O\rightarrow2H_3PO_4\)
CH4 +2O2 -t--> CO2 + 2H2O
C+O2 -t-> CO2
S + O2 -t--> SO2
4Al + 2O2 -t--> 2Al2O3
3Fe + 2O2 -t--> Fe3O4
b)
Fe2O3 + 3H2 -t-> 2Fe + 3H2O
HgO + H2 -t--> Hg + H2O
PbO + H2 -t--> H2O + Pb
c) 2Na + 2H2O --> 2NaOH + H2
CaO + H2O ---> Ca(OH)2
Na2O + H2O --> 2NaOH
SO2 + H2O ---> H2SO3
P2O5 + 3H2O --> 2H3PO4

\(n_{Fe}=\dfrac{2,8}{56}=0,05mol\)
\(\Rightarrow m_{Cu}=6-2,8=3,2g\)\(\Rightarrow n_{Cu}=0,05mol\)
\(CuO+H_2\rightarrow Cu+H_2O\)
0,05 0,05
\(Fe_2O_3+3H_2\rightarrow2Fe+3H_2O\)
0,075 0,05
\(\Rightarrow\Sigma n_{H_2}=0,075+0,05=0,125mol\)
\(\Rightarrow V=0,125\cdot22,4=2,8l\)

a) Fe2O3 + 3H2 → 2Fe + 3H2O.
b) HgO + H2 → Hg + H2O.
c) PbO + H2 → Pb + H2O.

\(PbO+H_2\rightarrow\left(t^o\right)Pb+H_2O\)
\(HgO+H_2\rightarrow\left(t^o\right)Hg+H_2O\)
\(FeO+H_2\rightarrow\left(t^o\right)Fe+H_2O\)
\(Fe_2O_3+3H_2\rightarrow\left(t^o\right)2Fe+3H_2O\)
\(Fe_3O_4+4H_2\rightarrow\left(t^o\right)3Fe+4H_2O\)

Gọi số mol CuO và Fe2O3 là a, b (mol)
=> 80a + 160b = 56 (1)
PTHH: CuO + H2 --to--> Cu + H2O
Fe2O3 + 3H2 --to--> 2Fe + 3H2O
CuO + CO --to--> Cu + CO2
Fe2O3 + 3CO --to--> 2Fe + 3CO2
=> 64a + 112b = 43,2 (2)
(1)(2) => a = 0,5 (mol); b = 0,1 (mol)
\(n_{H_2\left(lý.thuyết\right)}=n_{CO\left(lý.thuyết\right)}=a+3b=\)0,8 (mol)
=> \(n_{H_2\left(tt\right)}=n_{CO\left(tt\right)}=\dfrac{0,8.120}{100}=0,96\left(mol\right)\)
=> \(V_{H_2\left(tt\right)}=V_{CO\left(tt\right)}=0,96.22,4=21,504\left(l\right)\)


C âu 1
Lấy mẫu thử và đánh dấu
Cho lần lượt các khí trên vào que đóm đang cháy
+ Nếu là khí hi đro thì que đóm cháy lửa có màu xanh
+ nếu là oxi thì que đóm cháy mạnh hơn
+ Nếu là ko khí thì nó vân cháy bình thường
Câu 1 :
Cho tàn que đốm đỏ vào các lọ khí :
- Khí cháy với màu xanh nhạt : H2
- Bùng cháy : O2
- Tắt hẳn : không khí
Câu 2 :
\(Fe_2O_3+3H_2\underrightarrow{t^0}2Fe+3H_2O\)
\(CuO+H_2\underrightarrow{t^0}Cu+H_2O\)
\(HgO+H_2\underrightarrow{t^0}Hg+H_2O\)
\(FeO+H_2\underrightarrow{t^0}Fe+H_2O\)
\(PbO+H_2\underrightarrow{t^0}Pb+H_2O\)
\(Fe_3O_4+4H_2\underrightarrow{t^0}3Fe+4H_2O\)