Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án C.
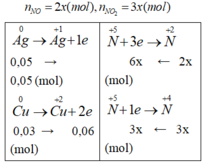
9x = 0,11; x= 11/900 => V = 5x.22,4 = 1,368 (l)

\(n_{HNO_3}=1.2\left(mol\right)\)
\(n_{NO}=a\left(mol\right)\)
\(n_{NO_2}=b\left(mol\right)\)
\(n_{N_2}=c\left(mol\right)\)
\(\Rightarrow a+b+c=\dfrac{5.6}{22.4}=0.25\left(1\right)\)
Bảo toàn e :
\(3\cdot0.2+1\cdot0.3=3a+b+10c\left(2\right)\)
\(n_{H^+}=4n_{NO}+2n_{NO_2}+12n_{N_2}\)
\(\Rightarrow4a+2b+12c=1.2\left(3\right)\)
\(\left(1\right),\left(2\right),\left(3\right):a=b=0.1,c=0.05\)
\(\%V_{NO_2}=\dfrac{0.1}{0.25}\cdot100\%=40\%\%0-\)

Ta có: \(n_{NO}+n_{NO_2}+n_{N_2}=\dfrac{22,4}{22,4}=1\left(mol\right)\left(1\right)\)
Mà: mX = 35,8 (g)
\(\Rightarrow30n_{NO}+46n_{NO_2}+28n_{N_2}=35,8\left(2\right)\)
Có: \(n_{Al}=\dfrac{32,4}{27}=1,2\left(mol\right)\)
\(n_{Cu}=\dfrac{22,4}{64}=0,35\left(mol\right)\)
BT e, có: 3nNO + nNO2 + 10nN2 = 3nAl + 2nCu = 4,3 (3)
Từ (1), (2) và (3) \(\Rightarrow\left\{{}\begin{matrix}n_{NO}=0,3\left(mol\right)\\n_{NO_2}=0,4\left(mol\right)\\n_{N_2}=0,3\left(mol\right)\end{matrix}\right.\)
⇒ nHNO3 = 4nNO + 2nNO2 + 12nN2 = 5,6 (mol)

a, BTNT N, có: nHNO3 (bị khử) = nNO + 2NN2O = 0,4 + 2.0,1 = 0,6 (mol)
b, Giả sử: nAl = mMg = x (mol)
Các quá trình:
\(Al^0\rightarrow Al^{+3}+3e\)
x___________ 3x (mol)
\(Mg^0\rightarrow Mg^{+2}+2e\)
x_____________ 2x (mol)
\(N^{+5}+3e\rightarrow N^{+2}\)
_____ 1,2 __ 0,4 (mol)
\(2N^{+5}+8e\rightarrow N_2^{+1}\)
_______0,8__0,1 (mol)
Theo ĐLBT mol e, có: 3x + 2x = 1,2 + 0,8 ⇒ x = 0,4 (mol)
⇒ nAl = nMg = 0,4 (mol)
BTNT Al, có: nAl(NO3)3 = nAl = 0,4 (mol)
BTNT Mg, có: nMg(NO3)2 = nMg = 0,4 (mol)
BTNT N, có: nHNO3 (pư) = 3nAl(NO3)3 + 2nMg(NO3)2 + nNO + 2nN2O
= 3.0,4 + 2.0,4 + 0,4 + 2.0,1 = 2,6 (mol)
c, m = mAl + mMg = 0,4.27 + 0,4.24 = 20,4 (g)
Bạn tham khảo nhé!

Coi \(n_{Cu} = n_{FeO} = 1(mol)\\ n_{Fe} = x(mol)\)
Bảo toàn electron cho quá trình 1:
\(2n_{Fe} + 2n_{Cu} = 3n_{NO}\)
⇒ 2x + 2 = 3a(1)
Y gồm \(Cu(NO_3)_2,Fe(NO_3)_2\)
Bảo toàn electron cho quá trình 2 :
\(n_{Fe(NO_3)_2} = x + 1 = 3n_{NO}\)
⇒ x + 1 = 3b(2)
Lấy (1) : (2), ta có \(\dfrac{2x + 2}{x + 1} =\dfrac{3a}{3b} \Rightarrow \dfrac{a}{b} = 2\)

Ta có: \(n_{Fe}=\dfrac{5,6}{56}=0,1\left(mol\right)\)
\(n_{Mg}=\dfrac{2,4}{24}=0,1\left(mol\right)\)
Theo ĐLBT e, có: 3nFe + 2nMg = nNO2 ⇒ nNO2 = 0,5 (mol)
BTNT Fe, có: nFe(NO3)3 = nFe = 0,1 (mol)
BTNT Mg, có: nMg(NO3)2 = nMg = 0,1 (mol)
BTNT N, có: nHNO3 = 3nFe(NO3)3 + 2nMg(NO3)2 + nNO2 = 1 (mol)

a)\(\left\{{}\begin{matrix}n_{Cu}=x\left(mol\right)\\n_{Al}=y\left(mol\right)\end{matrix}\right.\)
\(\Rightarrow\left\{{}\begin{matrix}64x+27y=9,1\\BTe:2x+3y=0,5\cdot1\end{matrix}\right.\Rightarrow\left\{{}\begin{matrix}x=0,1\\y=0,1\end{matrix}\right.\)
\(\%m_{Cu}=\dfrac{0,1\cdot64}{9,1}\cdot100\%=70,33\%\)
\(\%m_{Al}=100-70,33\%=29,67\%\)
b)\(\left\{{}\begin{matrix}n_{NO_2}+n_{NO}=0,5\\\dfrac{n_{NO_2}}{n_{NO}}=\dfrac{2}{1}\end{matrix}\right.\Rightarrow\left\{{}\begin{matrix}n_{NO_2}=\dfrac{1}{3}\\n_{NO}=\dfrac{1}{6}\end{matrix}\right.\)
Gọi \(\left\{{}\begin{matrix}n_{Cu}=a\left(mol\right)\\n_{Al}=b\left(mol\right)\end{matrix}\right.\)
\(\Rightarrow\left\{{}\begin{matrix}64a+27b=9,1\\BTe:2x+3y=\dfrac{1}{3}\cdot1+\dfrac{1}{6}\cdot3\end{matrix}\right.\Rightarrow\left\{{}\begin{matrix}a=\dfrac{4}{115}\\b=\dfrac{527}{2070}\end{matrix}\right.\)
\(\%m_{Cu}=\dfrac{\dfrac{4}{115}\cdot64}{9,1}\cdot100\%=24,46\%\)
\(\%m_{Al}=100\%-24,46\%=75,54\%\)
\(n_{HNO_3}=2n_{NO_2}+4n_{NO}=2\cdot\dfrac{1}{3}+4\cdot\dfrac{1}{6}=\dfrac{4}{3}mol\)

Chất rắn gồm : Ag,Cu dư
\(n_{Ag} = n_{AgNO_3} = 0,1(mol)\\ \Rightarrow n_{Cu} = \dfrac{15,92-0,1.108}{64} = 0,08(mol)\)
Gọi \(n_{Cu} = n_{Fe} = a(mol)\)
Dung dịch sau phản ứng :
\(Fe^{2+} : a + 0,14\\ Cu^{2+} : a - 0,08\\ NO_3^- : 0,1 + 0,14.3 = 0,52(mol)\)
Bảo toàn điện tích : 2(a+0,14) + 2(a -0,08) = 0,52
⇒ a = 0,1
Vậy \(n_{Fe^{2+}} = a + 0,14 = 0,24(mol)\)
Bảo toàn e :
\(n_{Fe^{2+}} = 3n_{NO}\\ \Rightarrow n_{NO} = \dfrac{0,24}{3} = 0,08(mol)\\ \Rightarrow V = 0,08.22,4 = 1,792(lít)\)
Đáp án C





Đặt $n_{NO}=2a(mol);n_{NO_2}=a(mol)$
Bảo toàn e ta có: $6a+a=0,1.3+0,25.3\Rightarrow a=0,15(mol)$
Do đó $n_{A}=0,15.3=0,45(mol)\Rightarrow V_A=10,08(l)$
tham khảo trong:
https://moon.vn/hoi-dap/hoa-tan-hoan-toan-hon-hop-gom-01-mol-fe-va-025-mol-al-vao-dung-dich-hno3-du-thu-duoc-530914