Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

\(m_{Br_2}=80g\Rightarrow n_{Br_2}=0,5mol\)
\(C_2H_4+Br_2\rightarrow C_2H_4Br_2\)
0,5 0,5
\(n_{hh}=\dfrac{28}{22,4}=1,25mol\)
\(\Rightarrow n_{CH_4}=1,25-0,5=0,75mol\)
\(\%V_{CH_4}=\dfrac{0,75}{1,25}\cdot100\%=60\%\)
\(\%V_{C_2H_4}=100\%-60\%=40\%\)

\(n_{Br_2}=\dfrac{m_{Br_2}}{M_{Br_2}}=\dfrac{16}{160}=0,1mol\)
\(C_2H_4+Br_2\rightarrow C_2H_4Br_2\)
0,1 0,1 ( mol )
\(\%V_{C_2H_4}=\dfrac{0,1.22,4}{16,8}.100=13,33\%\)
\(\%V_{CH_4}=100\%-13,33\%=86,67\%\)

a) \(n_{Br_2\left(p\text{ư}\right)}=\dfrac{6,4}{160}=0,04\left(mol\right);n_{hh}=\dfrac{13,44}{22,4}=0,6\left(mol\right)\)
PTHH: \(C_2H_4+Br_2\rightarrow C_2H_4Br_2\)
0,04<--0,04
\(\Rightarrow\left\{{}\begin{matrix}\%V_{C_2H_4}=\dfrac{0,04}{0,6}.100\%=6,67\%\\\%V_{CH_4}=100\%-6,67\%=93,33\%\end{matrix}\right.\)
b) \(n_{CH_4}=0,6-0,04=0,56\left(mol\right)\)
PTHH: \(CH_4+2O_2\xrightarrow[]{t^o}CO_2+2H_2O\)
0,56----------->0,56
\(C_2H_4+3O_2\xrightarrow[]{t^o}2CO_2+2H_2O\)
0,04----------->0,08
\(\Rightarrow V_{CO_2}=\left(0,08+0,56\right).22,4=14,336\left(l\right)\)

CH4+2O2-to>CO2+2H2O
x-----------------------------2x
C2H2+\(\dfrac{5}{2}\)O2-to>2CO2+H2O
y-----------------------------------y
=>\(\left\{{}\begin{matrix}x+y=\dfrac{3,36}{22,4}\\2x+y=\dfrac{4,5}{18}\end{matrix}\right.\)
=>\(\left\{{}\begin{matrix}x=0,1\\y=0,05\end{matrix}\right.\)
=>%VCH4=\(\dfrac{0,1.22,4}{3,36}\).100=66,67%
=>%VC2H2=100-66,67%=33,33%
b)
C2H2+2Br2->C2H2Br4
0,05-----0,1 mol
=>m Br2=0,1.160=16g

a) Khi cho metan và axetilen qua dung dịch brom thì metan không phản ứng với brom nên thoát ra khỏi bình còn axetilen phản ứng với dung dịch brom.
=> 20,16 lít khí thoát là metan CH4
=> V axetilen = 40,32 - 20,16 = 20,16 lít
<=> %V CH4 = %V C2H2 = 50%
b)
nCH4 = nC2H2 = \(\dfrac{20,16}{22,4}\)= 0,9 lít
CH4 + 2O2 → CO2 + 2H2O
C2H2 + \(\dfrac{5}{2}\)O2 → 2CO2 + H2O
Theo tỉ lệ phản ứng cháy => nO2 cần để đốt cháy hết hỗn hợp khí = 2nCH4+\(\dfrac{5}{2}\)nC2H2= 4,05 mol.
=> V O2 cần dùng = 4,05.22,4 = 90,72 lít

a, nBr2 = 8/160 = 0,05 (mol)
PTHH: C2H4 + Br2 -> C2H4Br2
Mol: 0,05 <--- 0,05 <--- 0,05
Vhh khí = 2,8/22,4 = 0,125 (mol)
%VC2H4 = 0,05/0,125 = 40%
%CH4 = 100% - 40% = 60%
b, nCH4 = 0,125 - 0,05 = 0,075 (mol)
PTHH: C2H4 + 3O2 -> (t°) 2CO2 + 2H2O
Mol: 0,05 ---> 0,15
CH4 + 2O2 -> (t°) CO2 + 2H2O
Mol: 0,075 ---> 0,15
Vkk = (0,15 + 0,15) . 5 . 22,4 = 33,6 (l)

Thể tích khí đã tác dụng với dung dịch brom là : 6,72 - 2,24 = 4,48 (lít).
=> Số mol khí phản ứng với dung dịch brom là : 4,48/22,4 = 0,2 mol
Khối lượng bình brom tăng lên là do khối lượng hiđrocacbon bị hấp thụ. Vậy khối lượng mol phân tử của hiđrocacbon là :
5,6/0,2 = 28 (gam/mol)
=> Công thức phân tử của một hiđrocacbon là C 2 H 4
Dựa vào phản ứng đốt cháy tìm được hiđrocacbon còn lại là CH 4
% V C 2 H 4 = 4,48/6,72 x 100% = 66,67%; V CH 4 = 33,33%

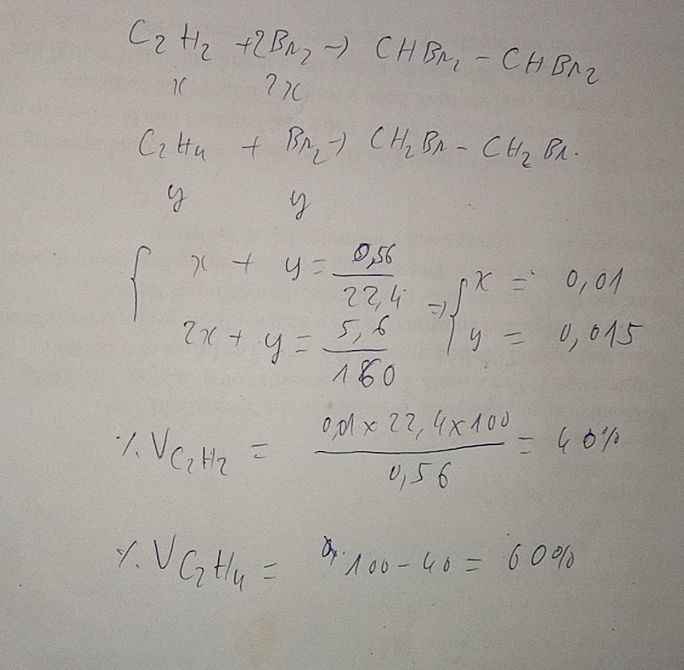

a)
\(n_{Br_2}=\dfrac{8}{160}=0,05\left(mol\right)\)
PTHH: C2H4 + Br2 --> C2H4Br2
0,05<-0,05
=> \(n_{CH_4}=\dfrac{3,36}{22,4}-0,05=0,1\left(mol\right)\)
\(\%m_{CH_4}=\dfrac{0,1.16}{0,1.16+0,05.28}.100\%=53,33\%\)
\(\%m_{C_2H_4}=\dfrac{0,05.28}{0,1.16+0,05.28}.100\%=46,67\%\)
b)
PTHH: CH4 + 2O2 --to--> CO2 + 2H2O
0,1-->0,2
C2H4 + 3O2 --to--> 2CO2 + 2H2O
0,05--->0,15
=> \(V_{O_2}=\left(0,2+0,15\right).22,4=7,84\left(l\right)\)