Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Phải dùng 4,2 g Fe
Cần 6g sắt (III) oxit tác dụng với H2 dư

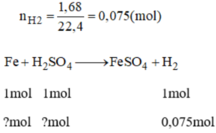
Theo phương trình phản ứng ta có:
n F e = n H 2 = 0,075 mol
n H 2 S O 4 = 0,075 mol (mà H 2 S O 4 đề cho là 0,2 mol nên H 2 S O 4 dư)
![]()

a, PT: \(Fe+H_2SO_4\rightarrow FeSO_4+H_2\)
b, Ta có: \(n_{H_2}=\dfrac{1,68}{22,4}=0,075\left(mol\right)\)
Theo PT: \(n_{Fe}=n_{H_2}=0,075\left(mol\right)\Rightarrow m_{Fe}=0,075.56=4,2\left(g\right)\)
c, \(n_{H_2SO_4\left(pư\right)}=n_{H_2}=0,075\left(mol\right)\Rightarrow n_{H_2SO_4\left(dư\right)}=0,2-0,075=0,125\left(mol\right)\)
\(\Rightarrow m_{H_2SO_4\left(dư\right)}=0,125.98=12,25\left(g\right)\)

a) Fe + 2HCl --> FeCl2 + H2
b) \(n_{H_2}=\dfrac{3,36}{22,4}=0,15\left(mol\right)\)
PTHH: Fe + 2HCl --> FeCl2 + H2
0,15<--------------------0,15
=> mFe =0,15.56 = 8,4 (g)

\(n_{H_2}=\dfrac{6,72}{22,4}=0,3mol\)
\(Fe+H_2SO_4\rightarrow FeSO_4+H_2\uparrow\)
0,3 0,3
a)\(m_{Fe}=0,3\cdot56=16,8g\)
b)\(Fe_2O_3+3H_2\rightarrow3Fe+3H_2O\)
0,1 0,3 0,3
\(m_{Fe_2O_3}=0,1\cdot160=16g\)
a)nH2 =6,72:22,4=0,3(mol)
PTHH Fe+H2SO4--->FeSO4+H2
theo pt , nFe = nH2 = 0,3 (mol)
=> mFe =n.M=0,3.56=16,8(g)
b) Ta có nH2=nFe=0,3(MOL)
Pthh: Fe2O3 + 3H2 ---> 2Fe + 3H2O
theo pt , nFe2O3=1/3 nH2=0,1(mol)
=> mFe2O3= n.M=0,1.(56.2+16.3)=16(g)
Vậy để có lượng sắt tham gia phản ứng trên phải có 16g Fe2O3 để tác dụng với H2

a. Để tính khối lượng HCl đã dùng, ta cần biết số mol của Al đã phản ứng với HCl. Ta sử dụng phương trình phản ứng:
2Al + 6HCl → 2AlCl3 + 3H2
Theo đó, 2 mol Al tương ứng với 6 mol HCl. Vậy số mol HCl cần để phản ứng với 2,7 g Al là:
n(HCl) = n(Al) x (6/2) = 2,7/(27x2) x 6 = 0,05 mol
Khối lượng HCl tương ứng là:
m(HCl) = n(HCl) x M(HCl) = 0,05 x 36,5 = 1,825 g
Vậy khối lượng HCl đã dùng là 1,825 g.
b. Theo phương trình phản ứng, 2 mol Al tạo ra 3 mol H2. Vậy số mol H2 tạo ra từ 2,7 g Al là:
n(H2) = n(Al) x (3/2) = 2,7/(27x2) x 3 = 0,025 mol
Theo định luật Avogadro, 1 mol khí ở ĐKTC chiếm thể tích 22,4 L. Vậy thể tích H2 thu được là:
V(H2) = n(H2) x 22,4 = 0,025 x 22,4 = 0,56 L
P.c. CuO + H2 → Cu + H2O
Khối lượng CuO cần để khử hết 0,025 mol H2 là:
n(CuO) = n(H2)/2 = 0,0125 mol
m(CuO) = n(CuO) x M(CuO) = 0,0125 x 79,5 = 0,994 g
Vậy để khử hết H2, ta cần dùng 0,994 g CuO. Nếu dùng toàn bộ lượng H2 bay ra, chất CuO sẽ bị khử hoàn toàn thành Cu và không còn chất nào còn dư.

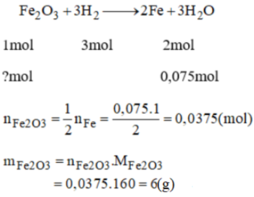


a, Ta có pt pư
\(Fe+H_2SO_4-->FeSO_4+H_2\)
Ta có
\(n_{H_2}=\dfrac{3,36}{22,4}=0,15\left(mol\right)\)
\(n_{H_2SO_4}=\dfrac{19,6}{98}=0,2\left(mol\right)\)
=> \(H_2SO_4\) dư
\(m_{H_2SO_4}=0,15\cdot98=14,7\left(g\right)\)
\(\Rightarrow m_{dư\left(H_2SO_4\right)}=19,6-14,7=4,9\left(g\right)\)
b,
Ta có
\(m_{Fe}=0,15\cdot56=8,4\left(g\right)\)
câu c đâu bạnn?