Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Vì Ag không tác dụng với H2SO4 loãng
Pt : \(2Al+3H_2SO_4\rightarrow Al_2\left(SO_4\right)_3+3H_2|\)
2 3 1 3
0,3 0,45
\a) Chất rắn không tan là Ag nên :
\(m_{Ag}=5,4\left(g\right)\)
⇒ \(m_{Al}=13,5-5,4=8,1\left(g\right)\)
0/0Al = \(\dfrac{8,1.100}{13,5}=60\)0/0
0/0Ag = \(\dfrac{5,4.100}{13,5}=40\)0/0
b) Có : \(m_{Al}=8,1\left(g\right)\)
\(n_{Al}=\dfrac{8,1}{27}=0,3\left(mol\right)\)
\(n_{H2}=\dfrac{0,3.3}{2}=0,45\left(mol\right)\)
\(V_{H2\left(dktc\right)}=0,45.22,4=10,08\left(l\right)\)
Chúc bạn học tốt

\(n_{H_2}=\dfrac{8,96}{22,4}=0,4\left(mol\right)\)
PTHH: Fe + H2SO4 → FeSO4 + H2
Mol: 0,4 0,4
\(m_{Fe}=0,4.56=22,4\left(g\right)\)
\(m_{hh}=22,4+5=27,4\left(g\right)\)
\(\%m_{Fe}=\dfrac{22,4.100\%}{27,4}=81,75\%;\%m_{Cu}=100-81,75=18,25\%\)

PTHH: \(Fe+H_2SO_4\rightarrow FeSO_4+H_2\uparrow\)
Dễ thấy \(m_{Cu}=12,8\left(g\right)\)
Ta có: \(n_{H_2}=\dfrac{13,44}{22,4}=0,6\left(mol\right)=n_{Fe}=n_{FeSO_4}=n_{H_2SO_4}\)
\(\Rightarrow\left\{{}\begin{matrix}m_{hh}=0,6\cdot56+12,8=46,4\left(g\right)\\C\%_{H_2SO_4}=\dfrac{0,6\cdot98}{196}\cdot100\%=30\%\\m_{FeSO_4}=0,6\cdot152=91,2\left(g\right)\\m_{H_2}=0,6\cdot2=1,2\left(g\right)\end{matrix}\right.\)
Mặt khác: \(m_{dd}=m_{hh}+m_{ddH_2SO_4}-m_{H_2}-m_{Cu}=228,4\left(g\right)\)
\(\Rightarrow C\%_{FeSO_4}=\dfrac{91,2}{228,4}\cdot100\%\approx39,93\%\)
\(Fe + H_2SO_4 \rightarrow FeSO_4 + H_2\)
Chất rắn không tan là Cu ( do Cu không pư \(H_2SO_4\))
\(n_{H_2} =\dfrac{13,44}{22,4}=0,6 mol\)
Theo PTHH
\(n_{Fe}= n_{H_2} = 0,6 mol\)
\(\Rightarrow m_{Fe} = 0,6 . 56=33,6g\)
\(m_{hh}= m_{Fe} + m_{Cu}= 33,6 + 12,8 =46,4g\)
b)
Theo PTHH
\(n_{H_2SO_4}=n_{H_2}= 0,6 mol\)
\(\Rightarrow m_{H_2SO_4}= 0,6 . 98=58,8g\)
C%\(H_2SO_4\)= \(\dfrac{58,8}{196} . 100\)%= 30%

Đáp án B
Phần chất rắn chưa tan là Al còn dư
Gọi n K = x mol
Cho hỗn hợp X vào nước, K phản ứng hết tạo KOH và Al phản ứng với KOH và còn dư => tính số mol theo KOH
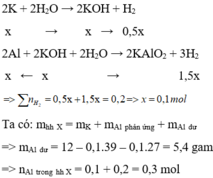
Cho hỗn hợp X tác dụng với dung dịch KOH dư => K phản ứng hết với H 2 O và Al phản ứng hết với KOH
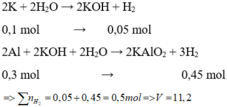

\(n_{H_2}=\dfrac{4,48}{22,4}=0,2\left(mol\right)\)
PTHH: Zn + 2HCl -->ZnCl2 + H2
____0,2<----------------------0,2
=> mZn = 0,2.65 = 13 (g)
mCu = mrắn không tan = 19,5 (g)
\(\left\{{}\begin{matrix}\%Zn=\dfrac{13}{13+19,5}.100\%=40\%\\\%Cu=\dfrac{19,5}{13+19,5}.100\%=60\%\end{matrix}\right.\)
`n_(H_2)=4,48/22,4=0,2 (mol)`
Ta có PTHH: `Zn+2HCl --> ZnCl_2 +H_2`
Theo PT: `1`--------------------------------`1`
Theo đề: `0,2`------------------------------`0,2`
`m_(Zn)=0,2.65=13(g)`
Vì `Cu` không phản ứng với `HCl` nên `m_(chất rắn không tan)=m_(Cu)=19,5(gam)`
`%Zn=13/(13+19,5) .100%=40%`
`%Cu=100%-40%=60%`




Chất rắn không tan là Al
$2Na + 2H_2O \to 2NaOH + H_2$
$2Al + 2NaOH + 2H_2O \to 2NaAlO_2 + 3H_2$
Theo PTHH :
$n_{H_2} =0,5n_{Na} + 1,5n_{NaOH} = 0,5n_{Na} + 1,5n_{Na} = 2n_{Na} = 0,2(mol)$
$\Rightarrow n_{Na} = 0,1(mol)$
$2Al + 3H_2SO_4 \to Al_2(SO_4)_3 + 3H_2$
$n_{Al} = \dfrac{3}{2}n_{H_2} = 0,1(mol)$
Suy ra:
$n_{Al\ đã\ dùng} = 0,1 + 0,1 = 0,2(mol)$
Suy ra:
$m_{hh} = 0,2.27 + 0,1.23 = 7,7(gam)$