Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

a) Phương trình hóa học của các phản ứng:
H2 + CuO → Cu + H2O (1).
3H2 + Fe2O3 → 2Fe + 3H2O (2).
b) Trong phản ứng (1), (2) chất khử H2 vì chiếm oxi của chất khác, chất oxi hóa là CuO và Fe2O3 vì nhường oxi cho chất khác.
c) Khối lượng đồng thu được từ 6g hỗn hợp 2 kim loại thu được:
mCu = 6g - 2,8g = 3,2g, nCu = 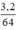 = 0,05 mol
= 0,05 mol
nFe = 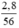 = 0,05 (mol)
= 0,05 (mol)
nH2 (1) = nCu = 0,05 mol ⇒ VH2(1) = 22,4 . 0,05 = 1,12 lít
nH2 (2) = 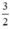 . nFe =
. nFe = 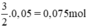 ⇒ VH2 (2) = 22,4 . 0,075 = 1,68 lít khí H2.
⇒ VH2 (2) = 22,4 . 0,075 = 1,68 lít khí H2.
VH2 = VH2(1) + VH2(2) = 1,12 + 1,68 = 2,8(l)

Câu 26:Oxi hóa hoàn toàn 8,4 gam một kim loại X chưa rõ hóa trị thu được 11,6 gam một oxit B. X là kim loại nào?
A. Cu. B. Na. C. Zn. D. Fe.
Câu 27:Công thức viết sai là:
A. MgO. B. FeO2. C. P2O5. D. ZnO.
Câu 28:Để đốt cháy hoàn toàn 2,4 gam kim loại magie thì thể tích không khí cần dùng là:
A. 2,24 lít. B. 11,2 lít. C. 22,4 lít. D. 5,6 lít.
Câu 29:Để oxi hóa hoàn toàn một kim loại R (hóa trị II) ta phải dùng một lượng oxi bằng 25% lượng kim loại đó. R là:
A. Fe. B. Pb. C. Ba. D. Cu.
Câu 30: Trong oxit, kim loại có hoá trị III và chiếm 70% về khối lượng là:
A. Cr2O3 B. Al2O3 C. As2O3 D. Fe2O3

Áp dụng ĐLBTKL, ta có:
mX + mO2 = mX2On
=> mO2 = 11,6 - 8,4 = 3,2 (g)
=> nO2 = 3,2/32 = 0,1 (mol)
PTHH: 4X + nO2 -> (t°) 2X2On
Mol: 0,4/n <--- 0,1
M(X) = 8,4/(0,4/n) = 21n (g/mol)
Xét:
n = 1 => Loại
n = 2 => Loại
n = 3 => Loại
n = 8/3 => X = 56 => X là Fe
Vậy X là Fe

a) PTHH:
CuO + H2 =(nhiệt)=> Cu + H2O (1)
Fe2O3 + 3H2 =(nhiệt)=> 2Fe + 3H2O (2)
b) - Dựa vào định nghĩa chất khử và chất oxi hóa
=> Chất khử: H2
Chất Oxi hóa: CuO và Fe2O3
c) Lượng đồng có trong 6g hỗn hợp 2 kim loại thu được:mCu = 6g - 2,8g = 3,2g.
VH2 cần dùng theo phương trình phản ứng(1) = \(\dfrac{3,2}{64}\cdot64=1,12\left(l\right)\) =
VH2 cần dùng theo phương trình phản ứng(2) = \(\dfrac{2,8}{56}\cdot\dfrac{3}{2}\cdot22,4=1,68\left(l\right)\)
a.Phương trình phản ứng:
CuO + H2 Cu + H2O (1)
1mol 1mol 1mol 1mol
Fe2O3 + 3H2 3H2O + 2Fe (2)
1mol 3mol 3mol 2mol
b. + Chất khử là H2 vì chiếm oxi của chất khác;
+ Chất oxi hóa: CuO, Fe2O3 vì nhường oxi cho chất khác.
c. Số mol đồng thu được là: nCu = = 0,5 (mol)
Số mol sắt là: nFe = = 0,05 (mol)
Thể tích khí H2 cần dùng để khử CuO theo phương trình phản ứng (1) là: nH2 = nCu = 0,05 mol => VH2 = 22,4.0,05 = 1,12 (lít)
Khí H2 cần dùng để khử Fe2O3 theo phương trình phản ứng (2) là:
nH2 = nFe =
.0,05 = 0,075 mol
=>VH2(đktc) = 22,4.0,075 = 1,68 (lít)

Bảo toàn khối lượng: mO2 = mRO - mR = 32,4 - 26 = 6,4 (g)
\(n_{O_2}=\dfrac{6,4}{32}=0,2\left(mol\right)\)
PTHH: 2R + O2 --to--> 2RO
\(M_R=\dfrac{26}{0,2}=65\left(\dfrac{g}{mol}\right)\)
=> R là Zn

a)
\(2R + O_2 \xrightarrow{t^o} 2RO\)
b)
Theo PTHH :
\(n_R = n_{RO} \)
⇔ \( \dfrac{3,6}{R} = \dfrac{6}{R+16}\)
⇔ R = 24(Mg)
Vậy kim loại R là Magie

$n_{H_2}=\dfrac{0,2}{2}=0,1(mol)$
$AO+H_2\xrightarrow{t^o}A+H_2O$
Theo PT: $n_A=n_{H_2}=0,1(mol)$
$\to M_A=\dfrac{6,4}{0,1}=64(g/mol)$
$\to A:Cu$
Vậy CT oxit là $CuO$

Bài 1:
\(n_M=\dfrac{16}{M_M}\left(mol\right)\)
PTHH: 2M + O2 --to--> 2MO
\(\dfrac{16}{M_M}\)---------->\(\dfrac{16}{M_M}\)
=> \(\dfrac{16}{M_M}\left(M_M+16\right)=20\)
=> MM = 64 (g/mol)
=> M là Cu
Bài 2:
\(n_R=\dfrac{16,2}{M_R}\left(mol\right)\)
PTHH: 2R + 3Cl2 --to--> 2RCl3
\(\dfrac{16,2}{M_R}\)------------>\(\dfrac{16,2}{M_R}\)
=> \(\dfrac{16,2}{M_R}\left(M_R+106,5\right)=80,1\)
=> MR = 27 (g/mol)
=> R là Al
1
ADDDLBTKL ta có
\(m_{O_2}=m_{MO}-m_M\\
m_{O_2}=20-16=4g\\
n_{O_2}=\dfrac{4}{32}=0,125\left(mol\right)\\
pthh:2M+O_2\underrightarrow{t^o}2MO\)
0,25 0,125
\(M_M=\dfrac{16}{0,25}=64\left(\dfrac{g}{mol}\right)\)
=> M là Cu
2
ADĐLBTKL ta có
\(m_{Cl_2}=m_{RCl_3}-m_R\\
m_{Cl_2}=80,1-16,2=63,9g\\
n_{Cl_2}=\dfrac{63,9}{71}=0,9\left(mol\right)\\
pthh:2R+3Cl_2\underrightarrow{t^o}2RCl_3\)
0,6 0,9
\(M_R=\dfrac{16,2}{0,6}=27\left(\dfrac{g}{mol}\right)\)
=> R là Al


Vậy B là Fe
==>Chọn C