Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

10 ml dung dịch RSO4 cần 0,003 mol BaCl2
![]() 50 ml dung dịch RSO4 cần 0,015 mol BaCl2
50 ml dung dịch RSO4 cần 0,015 mol BaCl2
![]() RSO4 = 1,8/0,015
RSO4 = 1,8/0,015 ![]() R = 24
R = 24
![]() R là Mg
R là Mg
![]() Chọn C
Chọn C

Cho dung dịch NaOH vào dung dịch muối sunfat của kim loại hóa trị II thấy sinh ra kết tủa tan trong dung dịch NaOH dư. Đó là muối nào sau đây?
A. MgSO4.
B. CaSO4.
C. MnSO4.
D. ZnSO4.
\(2NaOH+ZnSO_4\rightarrow Zn\left(OH\right)_2+Na_2SO_4\\ Zn\left(OH\right)_2+2NaOH\rightarrow Na_2ZnO_2+2H_2O\)

Đáp án D.
PTHH:
2NaOH + ZnSO4 → Na2SO4 + Zn(OH)2↓
Zn(OH)2 + 2NaOH → Na2ZnO2 + 2H2O

Gọi hóa trị của A là n(n\(\in\)Z;n>0)
\(n_{H_2SO_4}=0,15.0,2=0,03mol\\ A_2O_n+nH_2SO_4\rightarrow A_2\left(SO_4\right)_n+nH_2O\\ \Rightarrow\dfrac{2,4}{2A+16n}=\dfrac{0,03}{n}\Leftrightarrow0,06A+0,48b=2,4n\\ \Leftrightarrow0,06A=2,4n-0,48n\\ \Leftrightarrow0,06A=1,92n\\ \Leftrightarrow A=32n\)
| \(n\) | \(1\) | \(2\) | \(3\) |
| \(A\) | \(32\) | \(64\) | \(96\) |
| loại | nhận | loại |
Vậy kim loại A là đồng, Cu
\(n_{CuO}=\dfrac{2,4}{80}=0,03mol\\ CuO+H_2SO_4\rightarrow CuSO_4+H_2\\ n_{CuSO_4}=n_{CuO}=0,03mol\\ m_{CuSO_4}=0,03.160=4,8g\\ CTHH\left(B\right):CuSO_4.xH_2O\\ m_{H_2O.được.ngậm}=7,5-4,8=2,7g\\ \Rightarrow0,03.18x=2,7g\\ \Rightarrow x=5\\ \Rightarrow CTHH\left(B\right):CuSO_4.5H_2O\)

Chọn đáp án D.
► Xét thí nghiệm 1:
Quy quá trình về: X + 0,04 mol HCl + 0,08 mol NaOH.
⇒ nX = 0,08 – 0,04 = 0,04 mol
⇒ 250 ml dung dịch X chứa 0,2 mol H2RCOOH.
⇒ Mmuối = 35 ÷ 0,2 = 175 (H2NRCOOK)
⇒ R = 76 (-C6H4-)

Đáp án:C
Kết tủa Zn(OH)2 có tính lưỡng tính, tan trong NaOH dư.

Đáp án A
Tại catot có thể lần lượt xảy ra các quá trình:
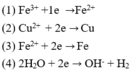
Tại anot có thể lần lượt xảy ra các quá trình:
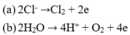
Sau khi điện phân A, cho dung dịch này phản ứng với NaOH thu được kết tủa B, nung B đến khối lượng không đổi thu được hỗn hợp 2 oxit. Trong A có 2 loại ion kim loại
Mặt khác, khi điện phân dung dịch A cho đến khi hết ion Cl - thì catot tăng 6,4 gam
⇒ Quá trình (2) đã xảy ra một phần, Cu 2 + vẫn còn trong dung dịch sau điện phân.
Gọi số mol Fe 3 + , Cu 2 + , Cl - , SO 4 2 - trong 100ml dung dịch A lần lượt là a,b,c,d.
Khi điện phân hết 
Theo bảo toàn e: số e do Fe3+ và Cu2+ nhận bằng số mol Cl- nhường. a + 0,1.2 = c (1)
Khối lượng dung dịch giảm gồm Cu2+ và Cl- đã phản ứng và bị tách ra khỏi dung dịch
6,4 + 35,5c = 17,05 (2)
Sau khi điện phân A, cho dung dịch này phản ứng với NaOH thu được kết tủa B, nung B đến khối lượng không đổi được 16 gam 2 oxit
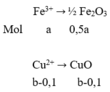
Suy ra: 160,0,5a + 80(b – 0,1) = 16 (3)
Theo định luật bảo toàn điện tích, đối với dung dịch A ta có:
3a + 2b = c + 2d (4)
Giải hệ phương trình ta được:
a = 0,1; b = 0,2; c= 0,3; d = 0,2
Khối lượng muối trong 100ml dung dịch A là 48,25 gam

Đáp án C
* Hỗn hợp gồm kim loại M, Fe, FeCO3 tác dụng với dung dịch HNO3 thu được 2 khí không màu trong đó có 1 khí hóa nâu ngoài không khí nên 2 khí là NO và CO2
Tính được nCO2=0,05 mol, n(NO)=0,15 mol nên n(FeCO3)=n(CO2)=0,05 mol.
Đặt nM=a mol, nên n(Fe)=b mol. Ta có: aM+56b+116.0,05=14,1
Nên aM+56b=8,3 (1)
- Dung dịch X2 có : a mol M(NO3)n; (b+0,05) mol Fe(NO3)3, HNO3 dư, có thể có c mol NH4NO3.
+ Phản ứng trung hòa:
HNO3+NaOH→NaNO3+H2O
n(NaOH)= n (HNO3dư)=0,2.1=0,2 mol
- dung dịch X3 có a mol M(NO3)n,( b+0,05) mol Fe(NO3)3, 0,2 mol NaNO3, có thể c mol NH4NO3.
* Cô cạn ½ dung dịch X3, tổng khối lượng chất rắn thu được là:
(M+62n)a+242(b+0,05)+80.c+85.0,2=38,3.2=76,6
aM+62an+242b+80c=47,5 (2)
* Cho dung dịch NaOH dư và ½ dung dịch X3 thu được kết tủa của một chất đó là Fe(OH)3
Fe(NO3)3+3NaOH→3NaNO3+Fe(OH)3
Ta có: 107(b+0,05)=16,05 suy ra b=0,1
Theo bảo toàn electron, ta có: an+ 0,3+0,05=0,45+8c suy ra an=0,1+8c (5)
Từ (1) suy ra aM=2,7 (6)
Từ (2) aM+62an+80c=23,3 (7)
Từ (5), (6), (7) an=0,3; c=0,025 M=9n n=3; M=27 là Al là nghiệm thỏa mãn.
n(HNO3 phản ứng)=nN(sp)=0,1.3+0,15.3+0,025.2+0,15=0,95mol
n(HNO3 bắt đầu)=0,95+0,2=1,15 mol x= CM(HNO3)=2,3M.


10 ml dung dịch RSO4 cần 0,15.0,02 = 0,003 mol BaCl2
⇒ 50 ml dung dịch RSO4 cần 0,015 mol BaCl2
⇒ R + 96 = 1,8/0,015 ⇒ R = 24 là Mg ⇒ Chọn C.