Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

a)Đặt 2 KL kiềm trên bằng KL M(I)
PTHH:
2M+2H20->2MOH+H2
Có:
nH2=1,12/22,4=0,05(mol)
Theo PTHH:
nM=2nH2=2.0,05=0,1(mol)
=> M=3,1/0,1=31(g)
Gỉa sử 2 ng tố cần tìm là X, Y
=> X<M<Y
=> X<31<Y
mà X, Y lại 2 chu kì liên tiếp
=> X, Y lần lượt là Na, K
b) PTHH:
2K+2H2O->2KOH+H2
x ---------------------> x/2 (mol)
2Na+2H2O->2NaOH+H2
y ----------------------> y/2 (mol)
Coi n K là x(mol)
n Na là y (mol)
Từ 2 PTHH trên ta có hpt:
39x+23y=3,1
x/2+y/2=0.05
=> x= 0,05 (mol)
y= 0.05 (mol)
PTHH:
NaOH +HCl-> NaCl+H2O
0,05 ---> 0,05 -> 0,05(mol)
KOH + HCl -> KCl+H2O
0,05 ---> 0,05 ->0,05 (mol)
Từ PTHH:
n HCl = 0,1(mol)
=> V HCl=0,1/2=0,05(l)
Có:
m NaCl= 0,05.58,5= 2,915(g)
m KCl= 0,05.74,5=3,725(g)

Gọi nM = x; nA = y; nB = z. M + 2H20 --> M(0H)2 + H2
x...........................x............
A + H20 --> A0H + 1/2H2 y.........................y........y/2
B + H20 --> B0H + 1/2H2 z......................z........z/2
Tổng n OH- là : 2x + y + z
1/2 dung dịch C thì chứa x + y/2 + z/2 mol 0H- chính bằng nH2 = 0,24 mol Ta có : H(+) + 0H(-) --->H20
0,24......0,24
=> tổng nH+ phải dùng là 0,24 mol (1)
mà số phân tử gam HCl nhiều gấp 4 lần số phân tử gam H2SO4. tức nHCl = 4nH2S04 nhưng trong phân tử H2S04 có 2H+
=> nH+ trong HCl = 2 nH+ trong H2S04 (2)
từ 1 và 2 => n H+ trong HCl =n Cl- = nHCl = 0,16 n H+ trong H2S04 = 2nS04(2-) =0,08
m muối = m kim loại + m Cl- + m S04(2-)
= 17,88/2 + 0,08*35,5 + 98*(0,08/2)
= 18,46 g
=> Đáp án D

Đáp án C
(*) Phương pháp: Bảo toàn khối lượng
-Lời giải:
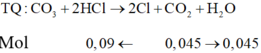
Bảo toàn khối lượng: mCacbonat + mHCl = mMuối Clorua + mCO2 + mH2O
⇒ m = 21 , 495 g

Chọn đáp án C
• muối cacbonat kim loại hóa trị II: MCO3 + 2HCl → MCl2 +CO2↑ + H2O
• muối cacbonat kim loại hóa trị I: N2CO3 + 2HCl → 2NCl + CO2↑ + H2O
từ tỉ lệ phản ứng có: ∑nHCl = 2∑nCO2↑ = 0,09 mol.
m gam muối khi cô cạn A là muối clorua, là sự thay thế 1 gốc CO32- bằng 2 gốc Cl.
⇒ tăng giảm khối lượng có: m = mmuối clorua = 21 + (0,09 × 35,5 – 0,045 × 60) = 21,495 gam.
⇒ Chọn đáp án C
21 + (0,09 × 35,5 – 0,045 × 60) tại sao có cái này vậy bạn? Sao lại lấy khối lượng muối clorua trừ khối lượng muối cacbonat rồi cộng với khối lượng hỗn hợp?



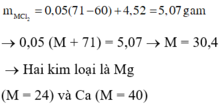




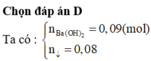


là hiđro và cacbon
Mg và Ca