Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

3Fe + 2O2 -> (t°) Fe3O4 (p/ư hóa hợp)
2Pb + O2 -> (t°) 2PbO (p/ư hoá hợp)
2KMnO4 -> (t°) K2MnO4 + MnO2 + O2 (p/ư phân hủy)
4Al + 3O2 -> (t°) 2Al2O3 (p/ư hoá hợp)
4K + O2 -> (t°) 2K2O (p/ư hoá hợp)
4P + 5O2 -> (t°) 2P2O5 (p/ư hoá hợp)
2KClO3 -> (t°, MnO2) 2KCl + 3O2 (p/ư phân hủy)
2Mg + O2 -> (t°) 2MgO (p/ư hoá hợp)
Hoàn thành pthh và phân loại phản ứng sau:
a)3Fe+2O2-to>...Fe3O4..- (pứ hóa hợp )
b)....2.Pb.+....O2...-to>2PbO (pứ hóa hợp )
c)2KMnO4-to>K2MnO4+.....MnO2.+O2 (pứ phân hủy)
d)Al+O2-to>....Al2O3 (pứ hóa hợp )
e)....4.K....+.....O2....-to>2K2O (pứ hóa hợp )
f)4P+5O2-to>..2P2O5.... (pứ hóa hợp )
g)2KClO3-to>2KCl+..3.O2.... (pứ phân hủy )
h)..2.Mg.....+.....O2....-to>2MgO (pứ hóa hợp )

phản ứng thế : Fe + CuCl2 → FeCl2 + Cu
Fe2O3+H2 Fe + H2O
Cu + AgNO3 → Ag + Cu(NO3)2
=> nguyên tố có độ hoạt động hóa học mạnh sẽ thay thế cho nguyên tố có độ hoạt động hóa học yếu hơn trong hợp chất của nguyên tố này

Câu 2: Cân bằng các phản ứng sau và phân loại phản ứng hóa hợp và phản ứng phân hủy?
A. 2Fe(OH)3 → Fe2O3 + 3H2O ( phân hủy)
B. CaO + CO2 → CaCO3 ( hóa hợp)
C. 4Al + 3O2 → 2Al2O3 ( Hóa hợp)
D. 2KClO3 → 2KCl + 3O2 ( phân hủy)
A. 2Fe(OH)3 → Fe2O3 + 3H2O.
→ Đây là phản ứng phân hủy.
B. CaO + CO2 → CaCO3.
→ Đây là phản ứng hóa hợp.
C. Al + O2 → Al2O3.
→ Đây là phản ứng hóa hợp.
D. KClO3 → KCl + O2.
→ Đây là phản ứng phân hủy.

1) 2H2O -điện phân---> 2H2+O2
O2 + 2Ca -t--> 2CaO
CaO +H2O ----> Ca(OH)2
2) 2KClO3 -t--> 2KClO3 + 3O2
O2 + 2Pb -t---> 2PbO
PbO + H2-t--> Pb+H2O
Pb+ HCl ---t--> PbCl2 + H2
3) 2KMnO4 -t--> K2MnO4 + MnO2 + O2
O2 + 2Hg -t--> 2HgO
HgO + H2 -t---> Hg+ H2O
4) 2H2O-điện phân--> 2H2+O2
H2 + FeO -t--> Fe + H2O
Fe + 2HCl ----> FeCl2+H2
H2+ ZnSO4 ---> H2SO4 +Zn
2Zn+ O2 -t--> 2ZnO
ZnO+ 2HCl -t--> ZnCl2 + H2O
5) O2 + H2----> H2O
H2O -điện phân---> H2+O2

\(1,4K+O_2\xrightarrow{t^o}2K_2O\\ 2,4P+5O_2\xrightarrow{t^o}2P_2O_5\\ 3,Fe_3O_4+4CO\xrightarrow{t^o}3Fe+4CO_2\\ 4,2KClO_3\xrightarrow[MnO_2]{t^o}2KCl+3O_2\\ 5,Ba+2H_2O\to Ba(OH)_2+H_2\\ 6,Fe_2O_3+3H_2\to 2Fe+3H_2O\\ 7,Na_2O+H_2O\to 2NaOH\\ 8,2Al+3H_2SO_4\to Al_2(SO_4)_3+3H_2\\ 9,2C_4H_{10}+13O_2\to 8CO_2+10H_2O\\ 10,2Al(OH)_3\xrightarrow{t^o}Al_2O_3+3H_2O\\ 11,C_5H_{12}+8O_2\xrightarrow{t^o}5CO_2+6H_2O\\ 12,2Al(OH)_3+3H_2SO_4\to Al_2(SO_4)_3+6H_2O\)

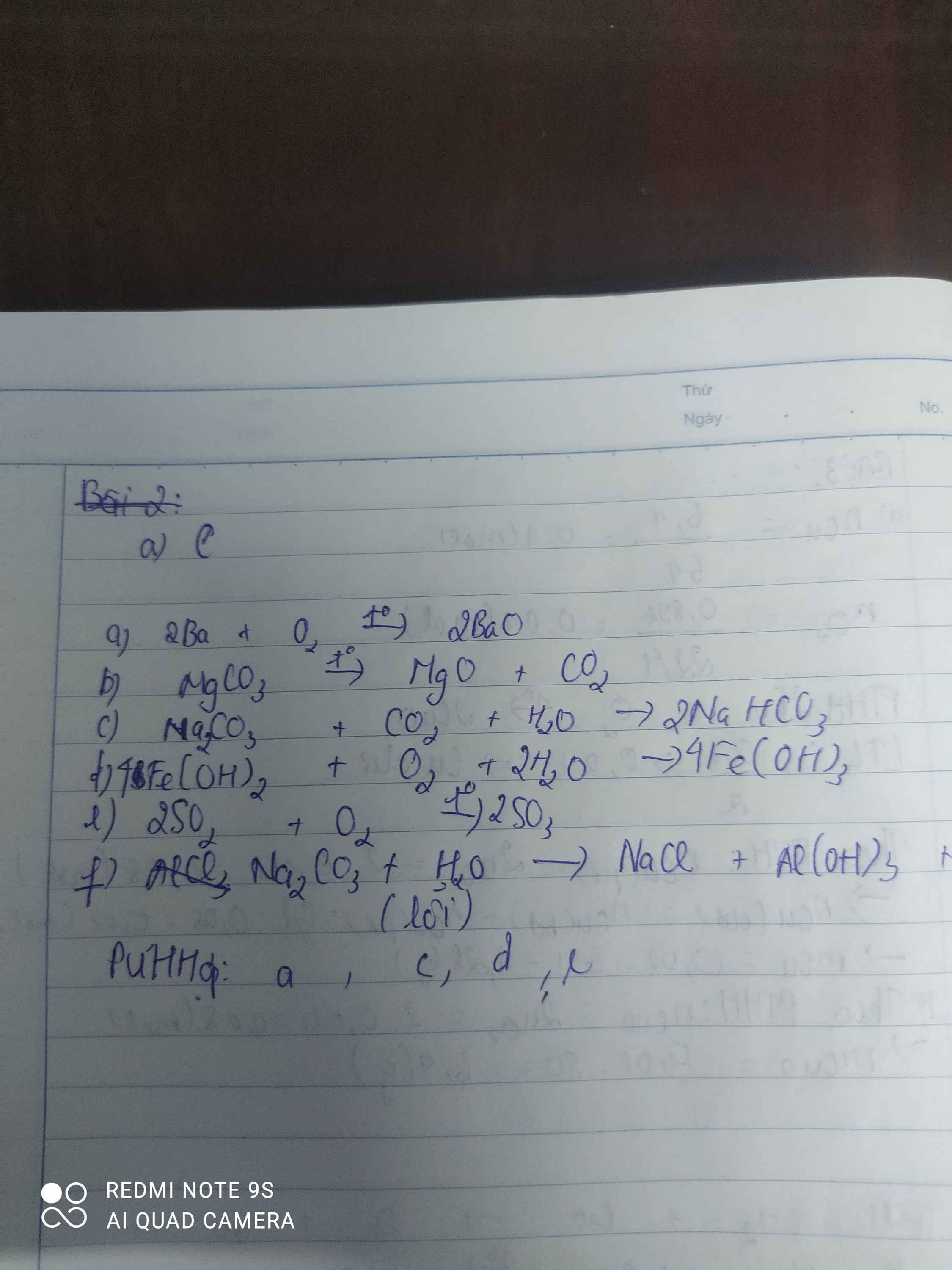

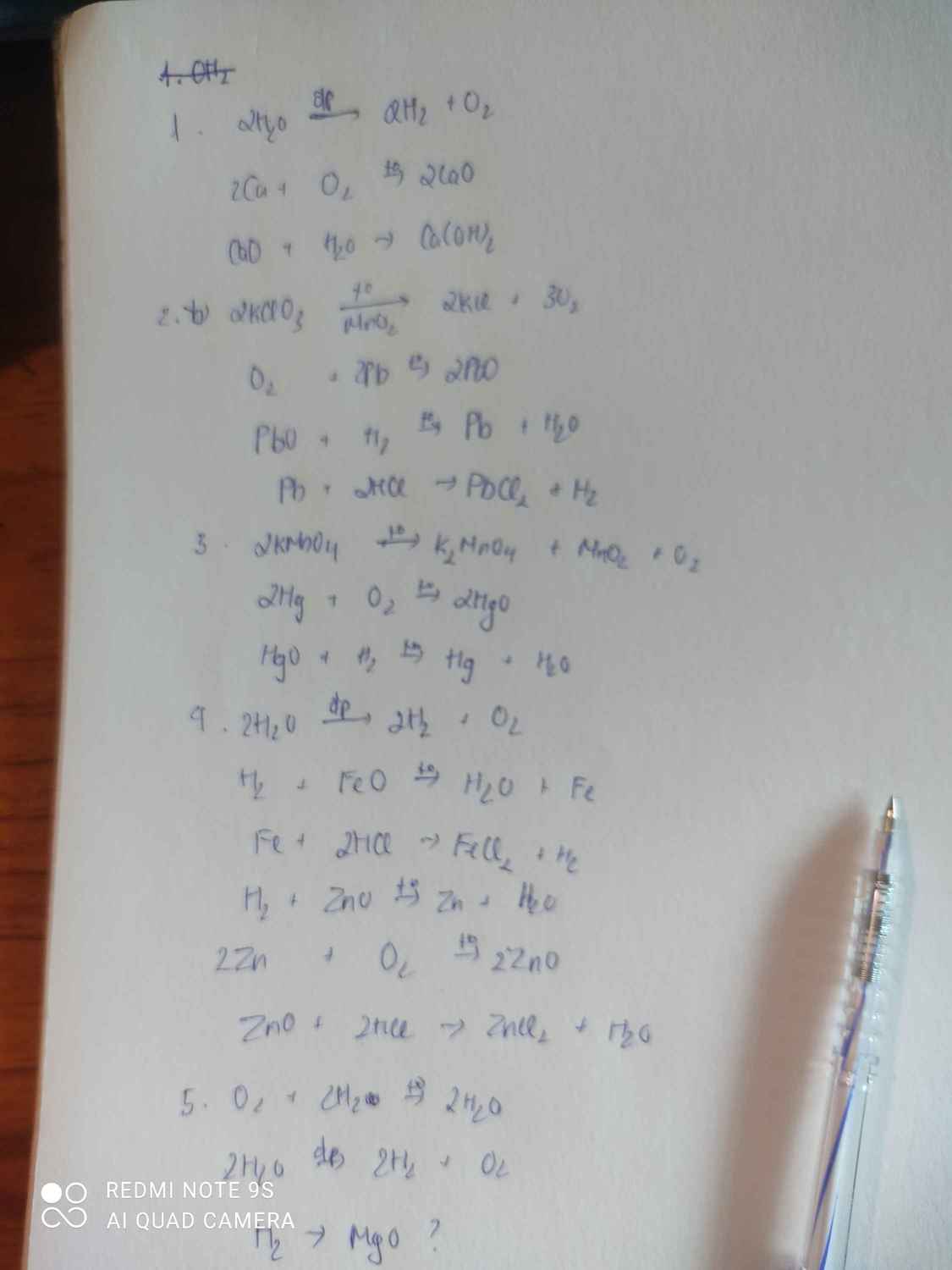

\(1,3Fe+2O_2\underrightarrow{t^o}Fe_3O_4\left(pư.hó.hợp\right)\\ 2,Fe_2O_3+3CO\underrightarrow{t^o}3Fe+3CO_2\uparrow\left(pư.oxi.hoá-khử\right)\\ 3,MgCO_3\underrightarrow{t^o}MgO+CO_2\uparrow\left(pư.phân.huỷ\right)\\ 4Fe\left(OH\right)_2+O_2+2H_2O\underrightarrow{t^o}4Fe\left(OH\right)_3\left(pư.hoá.hợp\right)\\ 2KClO_3\underrightarrow{t^o,MnO_2}2KCl+3O_2\uparrow\left(pư.phân.huỷ\right)\)
1. 3Fe + 2O2 \(\underrightarrow{t^o}\) Fe3O4 (hóa hợp)
2. Fe2O3 + 3CO → 2Fe + 3CO2(thế)
3. MgCO3→ MgO + CO2(phân hủy)
4. 4Fe(OH)2 + O2 + 2H2O → 4Fe(OH)3(hóa hợp)
5 . 2KClO3 → 2KCl + 3O2(phân hủy)