K
Khách
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.
Dưới đây là một vài câu hỏi có thể liên quan tới câu hỏi mà bạn gửi lên. Có thể trong đó có câu trả lời mà bạn cần!

24 tháng 11 2019
Chọn đáp án A
Đốt cháy 10,58g hỗn hợp X gồm 3 este đơn chức, mạch hở ta có: ![]() .
.
Mặt khác hidro hóa hoàn toàn 10,58 g hỗn hợp X cần 0,07 mol H2. Vậy 0,07 mol H2 chính là số mol liên kết π trong mạch Cacbon của 3 este.
![]()
Áp dụng định luật bảo toàn khối lượng cho phản ứng đốt cháy ta có:
![]()
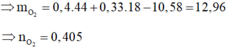
Áp dụng định luật bảo toàn nguyên tố O ta có:
![]()
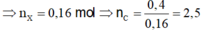
Vậy phải có 1 este có 2C. Vậy este đó phải là ![]() .
.
Theo đề bài ta thấy thủy phân Y trong NaOH chỉ thu được 1 ancol duy nhất, vậy ancol đó là CH3OH.
Vậy CT trung bình của 3 este sau khi hidro hóa là ![]() .
.
![]()
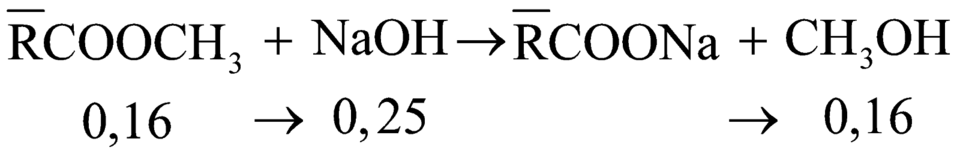
Áp dụng định luật bảo toàn khối lượng ta có:
![]()
![]()





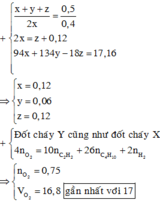

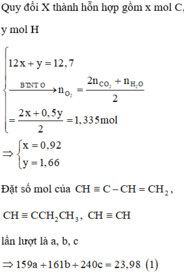
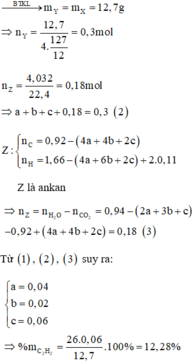
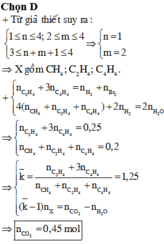

nCO2=0,4 mol
nH2O=0,5 mol
Đốt cháy hh sau khi cracking và đề hiđro hóa giống như đốt cháy C4H10 bđ=>nH2O-nCO2=nC4H10=0,1 mol
C4H10=>C3H6+CH4
x mol=>x mol =>x mol
C4H10=>C2H6+C2H4
y mol=>y mol =>y mol
C4H10=>C4H8 +H2
z mol=>z mol=>z mol
C4H10=>C4H6+2H2
t mol=>t mol
nBr2=0,12 mol=>x+y+z+2t=0,12
Tổng nC trong hh khí T=4x+4y+4z+4t=0,4=>x+y+z+t=0,1 mol
=>t=0,02 mol
=>%VC4H6=0,02/0,1.100%=20%
ANH GÌ ĐÓ ƠI GIÚP GIÙM EM BÀI NÀY VỚI Ạ!!!!
Trộn 500ml dd 0,2M với 200ml dd HCl 0,3M. Tính nồng độ mol của dung dịch HCl sau khi trộn