Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

\(m_{CuO}=50.20\%=10\left(g\right)\)
\(n_{CuO}=\dfrac{10}{80}=0,125\left(mol\right)\)
\(m_{Fe_2O_3}=50-10=40\left(g\right)\)
\(n_{Fe_2O_3}=\dfrac{40}{160}=0,25\left(mol\right)\)
PTHH :
\(CuO+H_2\underrightarrow{t^o}Cu+H_2O\)
0,125 0,125 0,125
\(Fe_2O_3+3H_2\underrightarrow{t^o}2Fe+3H_2O\)
0,25 0,75 0,5
\(a,V_{H_2}=\left(0,75+0,125\right).22,4=19,6\left(l\right)\)
\(b,m_{Cu}=0,125.64=8\left(g\right)\)
\(m_{Fe}=0,5.56=28\left(g\right)\)

\(\left\{{}\begin{matrix}m_{CuO}=50.20\%=10\left(g\right)\\m_{Fe_2O_3}=50-10=40\left(g\right)\end{matrix}\right.\Rightarrow\left\{{}\begin{matrix}n_{CuO}=\dfrac{10}{80}=0,125\left(mol\right)\\n_{Fe_2O_3}=\dfrac{40}{160}=0,25\left(mol\right)\end{matrix}\right.\)
PTHH:
\(CuO+H_2\xrightarrow[]{t^o}Cu+H_2O\)
0,125->0,125
\(Fe_2O_3+3H_2\xrightarrow[]{t^o}2Fe+3H_2\)
0,25--->0,75
\(\Rightarrow V_{H_2}=\left(0,75+0,125\right).22,4=18,2\left(l\right)\)

\(m_{CuO}=40.20\%=8\left(g\right)\)
\(n_{CuO}=\dfrac{8}{80}=0,1\left(mol\right)\)
\(n_{Fe_2O_3}=\dfrac{40-8}{160}=0,2\left(mol\right)\)
PTHH:
\(CuO+H_2\underrightarrow{t^o}Cu+H_2O\)
0,1 0,1
\(Fe_2O_3+3H_2\underrightarrow{t^o}2Fe+3H_2O\)
0,2 0,6
\(V_{H_2}=\left(0,1+0,6\right).22,4=15,68\left(l\right)\)

CHÚC BẠN HỌC TỐT![]()
a) Theo đề bài, ta có: \(n_{O2}=\dfrac{20}{32}=0,625\left(mol\right)\)
PTHH: \(2H_2+O_2\underrightarrow{o}2H_2O\)
pư............1.........0,5......1 (mol)
Ta có tỉ lệ: \(\dfrac{1}{2}< 0,625\). Vậy O2 dư, H2 hết.
\(\Rightarrow m_{H2O}=18.1=18\left(g\right)\)
Vậy.........

_ \(m_{Fe_2O_3}=0,8.50=40\left(g\right)\) \(\Rightarrow m_{CuO}=50-40=10\left(g\right)\)
_ \(n_{Fe_2O_3}=\dfrac{40}{160}=0,25mol\); \(n_{CuO}=\dfrac{10}{80}=0,125mol\)
PTHH: \(3H_2+Fe_2O_3\rightarrow2Fe+3H_2O\)
_____0,75mol_0,25mol
\(H_2+CuO\rightarrow Cu+H_2O\)
0,125__0,125 (mol)
\(\Rightarrow V_{H_2}=\left(0,75+0,125\right)22,4=19,6l\)

Ta có PTHH
CuO + H2 \(\rightarrow\) Cu + H2O (1)
Fe2O3 + 3H2 \(\rightarrow\) 2Fe + 3H2O (2)
mFe2O3 = 80% x 50 =40(g)
=> mCuO = 50 - 40 = 10(g)
=> nCuO = m/M = 10/80 = 0,125(mol)
nFe2O3 = m/M = 40/160= 0,25(mol)
Theo PT(1) => nH2 = nCuO = 0,125(mol)
Theo PT(2) => nH2 = 3 . nFe2O3 = 3 x 0,25 =0,75(mol)
=> tổng nH2 = 0,125 + 0,75 =0,875(mol)
=> VH2 = n x 22,4 = 0,875 x 22,4 =19,6(l)

mFe2O3=80%.50=40(g)
=>nFe2O3=40/160=0,25(mol)
mCuO=50-40=10(g)
=>nCuO=10/80=0,125(mol)
Fe2O3+3H2--t*-->2Fe+3H2O
0,75____0,75
CuO+H2--t*-->Cu+H2O
0,125__0,125
\(\Sigma H_2=\)0,75+0,125=0,875(mol)
=>VH2=0,875.22,4=19,6(l)

a) Phương trình hóa học của các phản ứng:
H2 + CuO → Cu + H2O (1).
3H2 + Fe2O3 → 2Fe + 3H2O (2).
b) Trong phản ứng (1), (2) chất khử H2 vì chiếm oxi của chất khác, chất oxi hóa là CuO và Fe2O3 vì nhường oxi cho chất khác.
c) Khối lượng đồng thu được từ 6g hỗn hợp 2 kim loại thu được:
mCu = 6g - 2,8g = 3,2g, nCu = 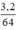 = 0,05 mol
= 0,05 mol
nFe = 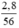 = 0,05 (mol)
= 0,05 (mol)
nH2 (1) = nCu = 0,05 mol ⇒ VH2(1) = 22,4 . 0,05 = 1,12 lít
nH2 (2) = 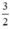 . nFe =
. nFe = 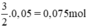 ⇒ VH2 (2) = 22,4 . 0,075 = 1,68 lít khí H2.
⇒ VH2 (2) = 22,4 . 0,075 = 1,68 lít khí H2.
VH2 = VH2(1) + VH2(2) = 1,12 + 1,68 = 2,8(l)



CuO+H2= Cu+H2O
Fe2O3+3H2=2Fe+3H2O
mFe2O3=\(\frac{50.20}{100}\)= 10g
nfe2o3= 10:56=0,18 mol
mcuo= 50-10=40 g
ncuo= 40:(64+16)=0,5 mol
theo pthh
nh2=3nfe2o3=0,54 mol
nh2=ncuo=0,5 mol
=>tông số mol h2= 0,5+0,54=1,04 mol
vh2=1,04.22,4=23,296 mol
các loại pư trên thuộc loại pư thế