Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

a) Hợp chất CO có MCO = 12 + 16 = 28 g/mol
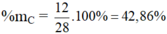
%mO = 100 – 42,86 = 57,14%
Hợp chất CO2: có MCO2 = 12 + 32 = 44 g/mol
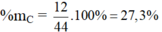
%mO = 100 – 27,3 = 72,7%
b) Hợp chất Fe3O4: MFe3O4 = 3.56 + 4.16 = 232 g/mol
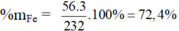
%mO = 100 – 72,4 = 27,6%
Hợp chất Fe2O3: MFe2O3 = 2.56 + 3.16 = 160 g/mol
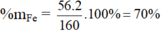
%mO = 100 – 70 = 30%
c) Hợp chất SO2 : MSO2 = 32 + 2.16 = 64 g/mol
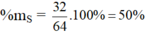
%mO = 100 – 50 = 50%
Hợp chất SO3 : MSO3 = 32 + 16.3 = 80 g/mol
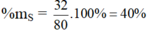
%mO = 100 – 40 = 60%

a) Với Fe3O4 thì Fe là 72,4% và O là 27,6%;
Với Fe2O3 thì Fe là 70% và O là 30%
b) Với SO2 thì S là 50% và O là 50%
Với SO3 thì S là 40% và O là 60%
c) mCu= \(\dfrac{80.80}{100}\)=64(g) ; mO=\(\dfrac{80.20}{100}\)=16(g)
nCu=\(\dfrac{64}{64}\)=1(mol) ; nO=\(\dfrac{16}{16}\)=1(mol)
Vậy CTHH của oxit đồng màu đen là: CuO
d) dA/H2=\(\dfrac{Ma}{2}\)=17 => MA=2.17=34(đvC)
H =\(\dfrac{5,88.34}{100}\)\(\approx\)2(đvC) ; S =\(\dfrac{94,12.34}{100}\)\(\approx\)32
=> CTHH của chất khí A là SH2

b. Ta có: \(\%_{Na}=100\%-60,68\%=39,32\%\)
Gọi CTĐG của A là: NaxCly
Ta lại có: \(\dfrac{x}{y}=\dfrac{\dfrac{39,32\%}{23}}{\dfrac{60,68\%}{35,5}}\approx\dfrac{1,7}{1,7}=\dfrac{1}{1}\Leftrightarrow\left\{{}\begin{matrix}x=1\\y=1\end{matrix}\right.\)
Gọi CTHH của A là: \(\left(NaCl\right)_n\)
Theo đề, ta có: \(M_{\left(NaCl\right)_n}=\left(23+35,5\right).n=58,5\)(g/mol)
\(\Leftrightarrow n=1\)
Vậy CTHH của A là NaCl
b. Gọi CTĐG của B là: \(Na_aC_bO_c\)
Ta có: \(x:y:z=\dfrac{43,4\%}{23}:\dfrac{11,3\%}{12}:\dfrac{45,3\%}{16}\approx1,9:0,9:2,8\approx2:1:3\)
Gọi CTHH của B là: \(\left(Na_2CO_3\right)_t\)
Theo đề, ta có: \(M_{\left(Na_2CO_3\right)_t}=\left(23.2+12+16.3\right).t=106\)(g/mol)
\(\Leftrightarrow t=1\)
Vậy CTHH của B là Na2CO3

\(PTK_{CuO}=64+16=80\left(đvC\right)\)
\(\%m_{Cu}=\) \(\dfrac{64}{80}.100=80\%\)
\(\%m_O=100-80=20\%\)
\(PTK_{MgCO_3}=24+12+3.16=84\left(đvC\right)\)
\(\%m_{Mg}=\dfrac{24}{84}.100=28,57\%\)
\(\%m_C=\dfrac{12}{84}.100=14,28\%\)
\(\%m_O=\dfrac{3.16}{84}.100=57,14\%\)
các ý còn lại làm tương tự

Câu 2:
Trong 1 mol X: \(\left\{{}\begin{matrix}n_{Ag}=\dfrac{170.63,53\%}{108}=1\left(mol\right)\\n_N=\dfrac{170.8,23\%}{14}=1\left(mol\right)\\n_O=\dfrac{170\left(100\%-63,53\%-8,23\%\right)}{16}=3\left(mol\right)\end{matrix}\right.\)
Vậy CTHH của X là \(AgNO_3\)
Câu 1:
\(a,\%_{Fe}=\dfrac{56}{180}\cdot100\%=31,11\%\\ \%_N=\dfrac{14\cdot2}{180}\cdot10\%=15,56\%\\ \%_O=100\%-31,11\%-15,56\%=53,33\%\\ b,\%_{N\left(N_2O\right)}=\dfrac{14\cdot2}{44}\cdot100\%=63,63\%\\ \%_{O\left(N_2O\right)}=100\%-63,63\%=36,37\%\\ \%_{N\left(NO\right)}=\dfrac{14}{30}\cdot100\%=46,67\%\\ \%_{O\left(NO\right)}=100\%-46,67\%=53,33\%\\ \%_{O\left(NO_2\right)}=\dfrac{16\cdot2}{46}\cdot100\%=69,57\%\\ \%_{N\left(NO_2\right)}=100\%-69,57\%=30,43\%\)

\(CaCO_3\\ \%m_{Ca}=\dfrac{40}{40+12+3.16}.100=40\%\\ \%m_C=\dfrac{12}{40+12+16.3}.100=12\%\\ \Rightarrow\%m_O=100\%-\left(40\%+12\%\right)=48\%\\ H_2SO_4\\ \%m_H=\dfrac{2.1}{2.1+32+4.16}.100\approx2,041\%\\ \%m_S=\dfrac{32}{2.1+32+4.16}.100\approx32,653\%\\ \%m_O=\dfrac{4.16}{2.1+32+4.16}.100\approx65,306\%\\ Fe_2O_3\\ \%m_{Fe}=\dfrac{56.2}{56.2+16.3}.100=70\%\\ \Rightarrow\%m_O=100\%-70\%=30\%\)
CaCO3
\(\%M_{\dfrac{Ca}{CaCO_3}}=\dfrac{40}{100}.100\%=40\%\)
\(\%M_{\dfrac{C}{CaCO_3}}=\dfrac{12}{100}.100\%=12\%\)
\(\%M_{\dfrac{O}{CaCO_3}}=100\%-\left(40\%+12\%\right)=48\%\)
H2SO4
\(\%M_{\dfrac{H_2}{H_2SO_4}}=\dfrac{2}{98}.100\%=2,04\%\)
\(\%M_{\dfrac{S}{H_2SO_4}}=\dfrac{32}{98}.100\%=32,65\%\)
\(\%M_{\dfrac{O}{H_2SO_4}}=100\%-\left(2,04\%+32,65\%\right)=65,31\%\)
Fe2O3
\(\%M_{\dfrac{Fe}{Fe_2O_3}}=\dfrac{112}{160}.100\%=70\%\)
\(\%M_{\dfrac{O}{Fe_2O_3}}=100\%-70\%=30\%\)

Khối lượng mol :
MKMnO4 = 39 + 55 + 64 = 158 (g/mol)
Số mol nguyên tử của mỗi nguyên tố có trong 1 mol hợp chất :
nK = 1 mol
nMn = 1 mol
nO = 4 mol
Khối lượng của mỗi nguyên tố có trong 1 mol hợp chất :
mK = 39.1 = 39 (g)
mMn = 55.1 = 55 (g)
mO = 16.4 = 64 (g)
Thành phần phần trăm theo khối lượng của mỗi nguyên tố trong hợp chất :
\(\%m_K=\frac{m_K}{M_{KMnO_4}}.100\%=\frac{39}{158}.100\%=24,7\%\)
\(\%m_{Mn}=\frac{m_{Mn}}{M_{KMnO_4}}.100\%=\frac{55}{158}.100\%=34,8\%\)
\(\%m_O=\frac{m_O}{m_{KMnO_4}}.100\%=\frac{64}{158}.100\%=40,5\%\)
Các bước giải bài toán xác định thành phần phần trăm theo khối lượng của các nguyên tố trong hợp chất khi biết công thức hoá học của hợp chất :
B1 : Tính khối lượng mol (M) của hợp chất.
B2 : Tính số mol nguyên tử của mỗi nguyên tố có trong 1 mol hợp chất.
B3 : Tính khối lượng của mỗi nguyên tố có trong 1 mol hợp chất.
B4 : Tính thành phần phần trăm theo khối lượng của mỗi nguyên tố trong hợp chất.

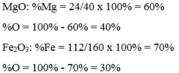

a/
+ CO
+CO2
b/
+Fe3O4
+ Fe2O3
c/
+SO2
+ SO3