Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Chọn A.
Hỗn hợp X gồm Mg (4x mol) và Fe (3x mol) và dung dịch chứa FeCl3 (6y mol) và CuCl2 (y mol)
Dung dịch Y chứa Fe2+, Mg2+ (4x mol) và Cl- (20y mol)


Tính toán theo PTHH :
Mg + CuSO4 → Cu + MgSO4
Mg + FeSO4 → Fe + MgSO4
Ba(OH)2 + MgSO4 → BaSO4 + Mg(OH)2
Ba(OH)2 + FeSO4 → BaSO4 + Fe(OH)2
Mg(OH)2 → MgO + H2O
2 Fe(OH)2 + ½ O2 → Fe2O3 + 2 H2O
Giả sư dung dịch muối phản ứng hết
=> n Fe = n FeSO4 = 0,2 . 1= 0,2 mol => m Fe = 0,2 . 56 = 11,2 g
=> n Cu =n CuSO4 = 0,2 . 0,5 = 0,1 mol => m Cu = 0,1 . 64 = 6,4 g
=> m chất rắn = 11,2 + 6,4 = 17,6 g > 12 g > 6,4
=> kim loại Fe dư sau phản ứng Vì CuSO4 phản ứng trước sau đó mới đến FeSO4 phản ứng
CuSO4 đã hết và phản ứng với 1 phần FeSO4
12 g = m Cu + m Fe phản ứng = 6,4 g + m Fe phản ứng
=> m Fe = 5,6 g => n Fe = 0,1 mol => n FeSO4 dư = 0,2 – 0,1 = 0,1 mol
Theo PTHH : n Mg = 0,1 + 0,1 = 0,2 mol ( bắng số mol CuSO4 và FeSO4 phản ứng )
Theo PTHH : n Mg = n MgSO4 = n Mg(OH)2 = n MgO = 0,2 mol
n FeSO4 dư = n Fe(OH)2 = n Fe2O3 . 2 = 0,1 mol
=> n Fe2O3 = 0,1 mol
=> m chất rắn = m Fe2O3 + m MgO = 0,1 . 160 + 0,2 . 40 = 24 g

\(n_{CuSO_4}=1.0,01=0,01(mol)\\ PTHH:Fe+CuSO_4\to FeSO_4+Cu\)
Do Cu ko td với HCl nên chất rắn sau phản ứng vẫn là Cu
\(n_{Cu}=n_{Fe}=0,01(mol)\\ \Rightarrow m_{Cu}=0,01.64=0,64(g)\\ b,PTHH:FeSO_4+2NaOH\to Fe(OH)_2\downarrow+Na_2SO_4\\ \Rightarrow n_{NaOH}=2n_{FeSO_4}=2n_{Fe}=0,02(mol)\\ \Rightarrow V_{dd_{NaOH}}=0,02.1=0,02(l)\)

Chọn đáp án B.
n A g N O 3 p h ả n ứ n g = 88 , 4 170 = 0 , 52 m o l
⇒ m A g C l m a x = 143 , 5 . 0 , 52 = 74 , 62 > 71 , 07
=> Chứng tỏ kết tủa gồm AgCl và Ag.
⇒ 143 , 5 n A g C l + 108 n A g = 71 , 07 g n A g C l + n A g = 0 , 52 m o l
⇒ n A g C l = 0 , 42 m o l n A g = 0 , 1 m o l
⇒ 2 n C u C l 2 + 3 n F e C l 3 = 0 , 42 m o l
n N a O H = 18 , 4 40 = 0 , 46 m o l
⇒ n A l C l 3 = n N a O H - n C l - = 0 , 04 m o l
⇒ n F e = 0 , 04 m o l
![]()
Chứng tỏ Fe và Al phản ứng hết.
⇒ n F e C l 3 = 0 , 06 m o l n C u C l 2 p ư = 0 , 07 m o l
![]()

Đáp án B
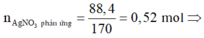
![]()
=> Chứng tỏ kết tủa gồm AgCl và Ag.
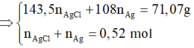
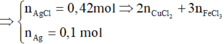
= 0,42 mol
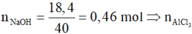
![]()
![]()
![]()
Chứng tỏ Fe và Al phản ứng hết.
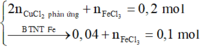
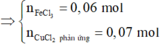
![]()

Câu 2:
\(n_{HCl}=0,18.1=0,18\left(mol\right)\\ 2Al+6HCl\rightarrow2AlCl_3+3H_2\\ n_{H_2\left(TT\right)}=\dfrac{1,512}{22,4}=0,0675\left(mol\right)\\ Vì:\dfrac{0,18}{6}>\dfrac{0,0675}{3}\Rightarrow Aldư\\ \Rightarrow n_{H_2\left(LT\right)}=\dfrac{0,18.3}{6}=0,09\left(mol\right)\\ H=\dfrac{0,0675}{0,09}.100\%=75\%\)
Câu 1:
a, \(Fe+CuSO_4\rightarrow FeSO_4+Cu\)
\(Fe+2HCl\rightarrow FeCl_2+H_2\)
Chất rắn còn lại sau pư là Cu.
Ta có: \(n_{CuSO_4}=0,01.1=0,01\left(mol\right)\)
Theo PT: \(n_{Cu}=n_{FeSO_4}=n_{CuSO_4}=0,01\left(mol\right)\Rightarrow m_{Cu}=0,01.64=0,64\left(g\right)\)
b, Dung dịch B: FeSO4
PT: \(FeSO_4+2NaOH\rightarrow Na_2SO_4+Fe\left(OH\right)_2\)
Theo PT: \(n_{NaOH}=2n_{FeSO_4}=0,02\left(mol\right)\)
\(\Rightarrow V_{NaOH}=\dfrac{0,02}{1}=0,02\left(l\right)\)



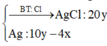
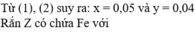



Ta có :
\(\text{nMg = 0,2 mol}\)
Do nồng độ FeCl2 gấp đôi CuCl2 nên ta đặt mol của CuCl2 và FeCl2 lần lượt là x, 2x (mol)
Các phản ứng theo thứ tự:
\(\text{(1) Mg + CuCl2}\rightarrow\text{MgCl2 + Cu}\)
\(\text{(2) Mg + FeCl2 }\rightarrow\text{MgCl2 + Fe}\)
TH1: Mg dư; CuCl2 và FeCl2 hết => nMg > nCuCl2 + nFeCl2
=> 0,2 > x + 2x => x < 0,2/3
\(\text{(1) Mg + CuCl2}\rightarrow\text{MgCl2 + Cu}\)
\(\text{x.................................. x}\)
\(\text{(2) Mg + FeCl2}\rightarrow\text{MgCl2 + Fe}\)
\(\text{2x .............................. 2x}\)
Kim loại sau phản ứng gồm: Cu (x mol); Fe (2x mol); Mg dư (0,2 - 3x mol)
=> m chất rắn = 64x + 56y + 24(0,2 - 3x) = 12 => x = 0,069 > 0,2/3 (loại)
\(\text{TH2: Mg hết; CuCl2 dư; FeCl2 chưa pư}\)
=> nMg < nCuCl2 => x > 0,2
\(\text{(1) Mg + CuCl2 }\rightarrow\text{MgCl2 + Cu}\)
\(\text{(2) Mg + FeCl2}\rightarrow MgCl2+Fe\)
\(\text{0,2-x →0,2-x 0,2-x 0,2-x}\)
Vậy chất rắn gồm: Cu (x mol); Fe (0,2-x mol)
=> m chất rắn = 64x + 56(0,2-x) = 12 => x = 0,1 (thỏa mãn)
\(\Rightarrow\text{V = nCuCl2 : CM CuCl2 = 0,1 : 1 = 0,1 lít = 100 ml}\)
Dung dịch B chứa: MgCl2 (0,2 mol); FeCl2 dư (0,1 mol)
{MgCl2, FeCl2} + NaOH dư → {Mg(OH)2, Fe(OH)2} Nung → MgO, Fe2O3
\(\text{BTNT "Mg": nMgO = nMgCl2 = 0,2 mol}\)
\(\text{BTNT "Fe": nFe2O3 = 0,5nFeCl2 = 0,05 mol}\)
\(\Rightarrow\text{y = mMgO + mFe2O3 = 0,2.40 + 0,05.160 = 16 gam}\)
ok đợi xíu nhéNhung Vũ