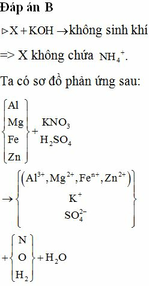
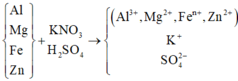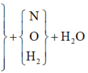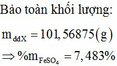Câu 9: Hòa tan 27 gam N2O5 vào 173 gam dung dịch KOH 28%.
1. Tính khối lượng muối tạo được.
2. Tính nồng độ % từng chất tan có trong dung dịch sau phản ứn
Câu 10: Hòa tan 8 gam MgO vào 100 gam dung dịch HNO3 12,6%. Tính nồng độ % của dung dịch thu được sau phản ứng.