Cho 20,5 gam hỗn hợp rượu etylic và axit axetic tác dụng với Kali dư thu được 4,48 lít khí H2 (đktc). Nếu cho hỗn hợp đó thực hiện phản ứng este hoá thì khối lượng este thu được là bao nhiêu?
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


PTHH: \(2C_2H_5OH+2Na\rightarrow2C_2H_5ONa+H_2\) (1)
\(2CH_3COOH+2Na\rightarrow2CH_3COONa+H_2\) (2)
a) Ta có: \(n_{H_2}=\frac{4,48}{22,4}=0,2\left(mol\right)\)
Đặt số mol của \(C_2H_5OH\) là \(a\) \(\Rightarrow n_{H_2\left(1\right)}=\frac{1}{2}a\)
Đặt số mol của \(CH_3COOH\) là \(b\) \(\Rightarrow n_{H_2\left(2\right)}=\frac{1}{2}b\)
Ta có hệ phương trình:
\(\left\{{}\begin{matrix}46a+60b=20,5\\\frac{1}{2}a+\frac{1}{2}b=0,2\end{matrix}\right.\) \(\Leftrightarrow\left\{{}\begin{matrix}a=0,25\\b=0,15\end{matrix}\right.\) \(\Rightarrow\left\{{}\begin{matrix}n_{C_2H_5OH}=0,25mol\\n_{CH_3COOH}=0,15mol\end{matrix}\right.\)
\(\Rightarrow m_{CH_3COOH}=60\cdot0,15=9\left(g\right)\)
\(\Rightarrow\%m_{CH_3COOH}=\frac{9}{20,5}\cdot100\approx43,9\%\)
\(\Rightarrow\%m_{C_2H_5OH}=56,1\%\)
b) PTHH: \(C_2H_5OH+CH_3COOH\underrightarrow{xt}CH_3COOC_2H_5+H_2O\)
Xét tỷ lệ: \(\frac{0,15}{1}< \frac{0,25}{1}\) \(\Rightarrow\) Axit phản ứng hết, Rượu còn dư
\(\Rightarrow n_{CH_3COOC_2H_5}=0,15mol\) \(\Rightarrow m_{este}=0,15\cdot88=13,2\left(g\right)\)
\(\Rightarrow m_{este}thực=13,2\cdot90\%=11,88\left(g\right)\)

Đáp án B
Gọi số mol của C2H5OH và CH3COOH lần lượt là x, y
Ta có hệ 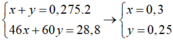
CH3COOH + C2H5OH ![]() CH3COOC2H5 + H2O
CH3COOC2H5 + H2O
Vì nCH3COOH > nC2H5OH nên hiệu suất được tính theo axit
Có neste = 0,2 mol → H = 0,2/0,25.100% = 80%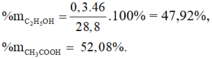

Chọn đáp án B
Gọi số mol của C2H5OH và CH3COOH lần lượt là x, y
Ta có hệ:
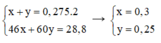
C H 3 C O O H + C 2 H 5 O H ⇌ C H 3 C O O C 2 H 5 + H 2 O
Vì n C H 3 C O O H < n C 2 H 5 O H nên hiệu suất được tính theo axit
Có neste = 0,2 mol
→ H = 0 , 2 0 , 25 × 100 % = 80 %
% m C 2 H 5 O H = 0 , 3 × 46 28 , 8 × 100 % = 47 , 92 % ,
% m C H 3 C O O H = 52 , 08 %

Lời giải
Xét thí nghiệm 1 ta có: n C H 3 C O O H = 0 , 2 ( m o l ) ; n C 2 H 5 O H = 1 , 05 ( m o l )
Ta có kết tủa là BaSO4 n B a S O 4 = 0 , 02 ( m o l ) ; n H 2 S O 4 = 0 , 02 ( m o l )
Có n C O 2 = 0 , 09 ( m o l ) trong X có CH3COOH dư;
n C H 3 C O O H d ư = n C O 2 - 2 n H 2 S O 4 = 0 , 05 ( m o l ) ⇒ n e s t e = n H 2 O = 0 , 2 - 0 , 05 = 0 , 15 ( m o l ) ⇒ m e s t e = 13 , 2 ( g ) ; n C 2 H 5 O H = 1 , 05 - 0 , 15 = 0 , 9 ( m o l )
=> Khi ở trạng thái cân bằng ta có K C = 0 , 15 . 0 , 15 0 , 9 . 0 , 05 = 0 , 5
Ở thí nghiệm 2 ta có:
n C H 3 C O O H = 0 , 16 ( m o l ) ; n C 2 H 5 O H = 0 , 32 ( m o l ) ; n H 2 O t r o n g d d a x i t 19 30 ( m o l )
Ở trạng thái cân bằng, gọi n e s t e = x ( m o l )
⇒ n C H 3 C O O H = 0 , 16 - x ( m o l ) ; n C 2 H 5 O H = 0 , 32 - x ( m o l ) n H 2 O = 19 30 + x ( m o l )
. Vì KC không đổi
⇒ x 19 30 + x ( 0 , 16 - x ) ( 0 , 32 - x ) = 0 , 5 ⇒ x = 0 , 29
Vậy meste = 2,552(g)
Đáp án C.

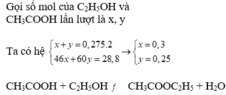


Gọi \(\left\{{}\begin{matrix}n_{ancol}:x\left(mol\right)\\n_{axit}:y\left(mol\right)\end{matrix}\right.\)
PTHH:
\(C_2H_5OH+K\rightarrow C_2H_5ONa+\frac{1}{2}H_2\)
x_____________________________0,5x
\(CH_3COOH+K\rightarrow CH_3COONa+\frac{1}{2}H_2\)
y____________________________________0,5y
Giải hệ PT:
\(\left\{{}\begin{matrix}46x+60y=20,5\\0,5x+0,5y=\frac{4,48}{22,4}=0,2\end{matrix}\right.\Rightarrow\left\{{}\begin{matrix}x=0,25\\y=0,15\end{matrix}\right.\)
\(PTHH:C_2H_5OH+CH_3COOH⇌CH_3COOC_2H_5+H_2O\)
\(\Rightarrow n_{CH3COOC2H5}=n_{CH3COOH}=0,15\left(mol\right)\)
\(\Rightarrow m_{este}=13,2\left(g\right)\)