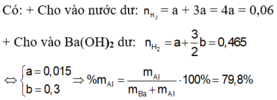Cho 9,6 gam hỗn hợp gồm Ca và CaO hòa tan hết vào nước, thu được 2,24 lít khí H 2 (đktc).
Viết phản ứng xảy ra.
Tính thành phần phần trăm theo khối lượng mỗi chất trong hỗn hợp ban đầu.
Tính khối lượng C a ( O H ) 2 thu được.
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.



\(n_{H_2}=\dfrac{2,24}{22,4}=0,1\left(mol\right)\)
PTHH:
Ca + 2H2O ---> Ca(OH)2 + H2
0,1<-------------0,1<---------0,1
=> \(\left\{{}\begin{matrix}m_{Ca}=0,1.40=4\left(g\right)\\m_{CaO}=9,6-4=5,6\left(g\right)\end{matrix}\right.\)
=> \(\left\{{}\begin{matrix}\%m_{Ca}=\dfrac{4}{9,6}.100\%=41,67\%\\\%m_{CaO}=100\%-41,67\%=58,33\%\end{matrix}\right.\)
\(n_{CaO}=\dfrac{5,6}{56}=0,1\left(mol\right)\)
PTHH: CaO + H2O ---> Ca(OH)2
0,1------------------>0,1
=> \(m_{Ca\left(OH\right)_2}=\left(0,1+0,1\right).74=14,8\left(g\right)\)

a. PTHH:
\(Ca+2H_2O--->Ca\left(OH\right)_2+H_2\left(1\right)\)
\(CaO+H_2O--->Ca\left(OH\right)_2\left(2\right)\)
b. Ta có: \(n_{H_2}=\dfrac{2,24}{22,4}=0,1\left(mol\right)\)
Theo PT(1): \(n_{Ca}=n_{H_2}=0,1\left(mol\right)\)
\(\Rightarrow m_{Ca}=0,1.40=4\left(g\right)\)
\(\Rightarrow\%_{m_{Ca}}=\dfrac{4}{9,6}.100\%=41,7\%\)
\(\%_{m_{CaO}}=100\%-41,7\%=58,3\%\)
c. Ta có: \(n_{CaO}=\dfrac{9,6-4}{56}=0,1\left(mol\right)\)
Ta có: \(n_{hh}=0,1+0,1=0,2\left(mol\right)\)
Theo PT(1,2): \(n_{Ca\left(OH\right)_2}=n_{hh}=0,2\left(mol\right)\)
\(\Rightarrow m_{Ca\left(OH\right)_2}=0,2.74=14,8\left(g\right)\)

\(n_{H_2}=\dfrac{2,24}{22,4}=0,1mol\)
\(Fe+2HCl\rightarrow FeCl_2+H_2\)
0,1 0,1 ( mol )
( Cu không tác dụng với dd axit HCl )
\(m_{Fe}=0,1.56=5,6g\)
\(\rightarrow m_{Cu}=12-5,6=6,4g\)
\(\rightarrow\left\{{}\begin{matrix}\%m_{Fe}=\dfrac{5,6}{12}.100=46,66\%\\\%m_{Cu}=100\%-46,66\%=53,34\%\end{matrix}\right.\)

150ml = 0,15l
Số mol của kali hidroxit
CMKOH = \(\dfrac{n}{V}\Rightarrow n=C_M.V=0,2.0,15=0,03\left(mol\right)\)
Pt : K2O + H2O \(\rightarrow\) 2KOH\(|\)
1 1 2
0,015 0,03
a) Số mol của kali oxit
nK2O = \(\dfrac{0,03.1}{2}=0,015\left(mol\right)\)
Khối lượng của kali oxit
mK2O= nK2O . MK2O
= 0,015 . 94
= 1,41 (g)
Khối lượng của đồng (II) oxit
mCuO = 13 - 1,41
= 11,59 (g)
b) 0/0K2O = \(\dfrac{m_{K2O}.100}{m_{hh}}=\dfrac{1,41.100}{13}=10,85\)0/0
0/0CuO = \(\dfrac{m_{CuO}.100}{m_{hh}}=\dfrac{11,59.100}{13}=89,15\)0/0
c) Có : mCuO = 11,59 (g)
số mol của đồng (II) oxit
nCuO = \(\dfrac{m_{CuO}}{M_{CuO}}=\dfrac{11,59}{80}=0,14\left(mol\right)\)
Pt : CuO + H2SO4 → CuSO4 + H2O\(|\)
1 1 1 1
0,14 0,14
K2O + H2SO4 → K2SO4 + H2O\(|\)
1 1 1 1
0,015 0,015
Số mol tổng của axit sunfuric
nH2SO4 = 0,14 + 0,015
= 0,155 (mol)
Khối lượng của axit sunfuric
mH2SO4 = nH2SO4 . MH2SO4
= 0,155 . 98
= 15,19 (g)
Khối lượng của dung dịch axit sunfuric
C0/0H2SO4 = \(\dfrac{m_{ct}.100}{m_{dd}}\Rightarrow m_{dd}=\dfrac{m_{ct}.100}{C}=\dfrac{15,19.100}{20}=\) 75,95 (g)
Thể tich của dung dịch axit sunfuric cần dùng
D = \(\dfrac{m}{V}\Rightarrow V=\dfrac{m}{D}=\dfrac{75,95}{1,143}=66,45\left(ml\right)\)
Chúc bạn học tốt

Đáp án C
Các phản ứng xảy ra:
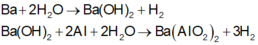
Khi cho m gam X tác dụng với dung dịch Ba (OH)2 dư thu được 20,832/2=10,416 lít H2 (đktc)
Vì thể tích H2 thu được ở hai trường hợp (khi sử dụng cùng khối lượng hỗn hợp X) khác nhau nên khi hòa tan hỗn hợp vào nước thì còn một phần kim loại Al dư không tan.
Trong m gam X gọi n Ba = a n Al = b