Xét phản ứng: SO 2 ( k ) + O 2 ( k ) ⇌ SO 3 ( k ) ; ( ∆ H < 0 ) . Để thu được nhiều SO 3 ta cần
A. thêm xúc tác
B. giảm áp suất
C. tăng nhiệt độ
D. giảm nhiệt độ
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.




Câu 1 :
b)
Cho quỳ tím ẩm vào mẫu thử
- mẫu thử hóa đỏ là P2O5
P2O5 + 3H2O $\to$ 2H3PO4
- mẫu thử hóa xanh là Na2O,CaO
Na2O + H2O $\to $ 2NaOH
CaO + H2O $\to$ Ca(OH)2
- mẫu thử không đổi màu là NaCl
Cho hai mẫu thử còn vào dung dịch H2SO4
- mẫu thử tạo kết tủa trắng là CaO
CaO + H2SO4 $\to$ CaSO4 + H2O
- mẫu thử không hiện tượng là Na2O
Câu 2 :
1)
\(S_{Na_2SO_4} = \dfrac{m_{Na_2SO_4}}{m_{H_2O}}.100 = \dfrac{7,2}{80}.100\% = 9(gam)\\ C\%_{Na_2SO_4} = \dfrac{S}{S + 100}.100\% = \dfrac{9}{100 + 9}.100\% = 8,26\%\)

Lập phương trình hóa học của các phản ứng sau
a)Al + CuCl2 ---> AlCl3 + Cu
2Al + 3CuCl2 → 2AlCl3 + 3Cu
b) K + O2 ---> K2O
4K + O2 → 2K2O
c) NaOH + Fe2 (SO4)3 ---> Fe ( OH)3 + Na2SO4
6NaOH + Fe2(SO4)3 → 2Fe(OH)3 + 3Na2SO4
PTHH
a)Al + CuCl2 ---> AlCl3 + Cu
2Al + 3CuCl2 → 2AlCl3 + 3Cu
b) K + O2 ---> K2O
4K + O2 → 2K2O
c) NaOH + Fe2 (SO4)3 ---> Fe(OH)3 + Na2SO4
6NaOH + Fe2(SO4)3 → 2Fe(OH)3 + 3Na2SO4

H2SO4 + Na2SO3 -> Na2SO4 + SO2 + H2O
SO2 + K2O -> K2SO3
K2SO3 + H2SO4 -> K2SO4 + SO2 + H2O
K2SO4 + BaCl2 -> BaSO4 + 2KCl

Đáp án B
CO(k) + H2O(h) D CO2(k) + H2(k)
Ban đầu 1 1 0 0(mol)
Phản ứng 2/3 2/3 ß 2/3 2/3(mol)
Cân bằng 1/3 1/3 2/3 2/3(mol)
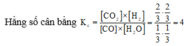

Đáp án B
Cân bằng chuyển dịch theo chiều thuận: hạ nhiệt độ thì
∆
H
<
0
; tăng áp suất thì
n
t
>
n
8
Chỉ có 2 và 3 thỏa mãn
Chọn B

a/ Na2O + H2O → 2NaOH (Phản ứng hóa hợp)
b/ 2KOH + H2SO4 → K2SO4 + 2H2O (Phản ứng oxi-hóa khử)
c/ 2SO2 + O2 → 2SO3 (Phản ứng oxi-hóa)
d/ 2Al2O3 → 4Al + 3O2 (Phản ứng phân hủy)

1. 2Cr +3 Cl2 → 2CrCl3
2. 4K + O2 → 2K2O
3. Mg + 2HCl → MgCl2 + H2
4. Fe2O3 + 3H2SO4 → Fe2(SO4)3 + 3H2O
a) 2Cr + 3Cl2 -> 2CrCl3
b) 4K + O2 -> t0 2K2O
c) Mg + 2HCl -> MgCl2 + H2
d) Fe2O3 + 3H2SO4 -> Fe2(SO4)3 + 3H2O