Cho 6,16 lít khí NH3 (đktc) và V ml dung dịch H3PO4 0,1M phản ứng hết với nhau thu được dung dịch X. X phản ứng được với tối đa 300 ml dd NaOH 1M. Khối lượng muối khan có trong X là
A. 13,325 gam.
B. 147,000 gam.
C. 14,900 gam
D. 14,475 gam.
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án C.
n(NH3) = 6,16/22,4 = 0,275mol
n(NaOH) = 1.0,3 = 0,3mol
Dung dịch X phản ứng tối đa với NaOH nên muối thu được là muối Na3PO4
Theo ĐL bảo toàn nguyên tố:
n(H3PO4) = n(Na3PO4) = n(NaOH) / 3 = 0,3/3 = 0,1mol
n(NH3) / n(H3PO4) = 0,275 / 0,1 = 2,75
2 < n(NH3) / n(H3PO4)< 3 → cả 2 chất đều tham gia pư hết
Theo ĐL bảo toàn khối lượng, khối lượng muối thu được là:
m(muối) = m(NH3) + m(H3PO4) = 17.0,275 + 98.0,1 = 14,475g

Chọn đáp án A
Chú ý tỉ lệ dung dich X trong mỗi phản ứng
Gọi số mol ion Na+, NH4+, CO32- và SO42- trong 100ml lần lượt a, b, c, d mol
Khi cho X tác dụng với HCl chỉ có CO32- tham gia phản ứng → c = 0,1 mol
Khi cho X tác dụng với BaCl2 thu được BaCO3 và BaSO4 → 0,1.197 + d.233= 43 → d = 0,1 mol
Khi cho X tác dụng lượng dư dung dịch NaOH chỉ có NH4+ tham gia phản ứng → b = 0,2 mol
Bảo toàn điện tích trong dung dịch X → a = 2. 0,1 + 2. 0,1 -0,2 = 0,2 mol
Vậy trong 300ml dung dịch X gồm 0,6 mol Na+, 0,6 mol NH4+, 0,3 mol CO32- và 0,3 mol SO42-
→ m = 0,6.23 + 0,6. 18 + 0,3. 60 + 0,3. 96= 71,4 gam.
Đáp án A.

Chọn đáp án A
Chú ý tỉ lệ dung dich X trong mỗi phản ứng
Gọi số mol ion Na+, NH4+, CO32- và SO42- trong 100ml lần lượt a, b, c, d mol
Khi cho X tác dụng với HCl chỉ có CO32- tham gia phản ứng → c = 0,1 mol
Khi cho X tác dụng với BaCl2 thu được BaCO3 và BaSO4 → 0,1.197 + d.233= 43 → d = 0,1 mol
Khi cho X tác dụng lượng dư dung dịch NaOH chỉ có NH4+ tham gia phản ứng → b = 0,2 mol
Bảo toàn điện tích trong dung dịch X → a = 2. 0,1 + 2. 0,1 -0,2 = 0,2 mol
Vậy trong 300ml dung dịch X gồm 0,6 mol Na+, 0,6 mol NH4+, 0,3 mol CO32- và 0,3 mol SO42-
→ m = 0,6.23 + 0,6. 18 + 0,3. 60 + 0,3. 96= 71,4 gam.
Đáp án A.

Chọn A
Gọi số mol Na + , NH 4 + , CO 3 2 - và SO 4 2 - trong 100ml dung dịch X lần lượt là x, y, z và t.
Bảo toàn điện tích có: x + y – 2z – 2t = 0 (1)
Cho 100ml X tác dụng với HCl dư:
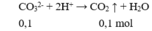
→ z = 0,1 (2)
Cho 100ml X tác dụng với BaCl2 dư:
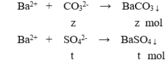
m↓ = 43 (gam) → 197z + 233t = 43 (3)
Cho 100 ml X tác dụng với NaOH
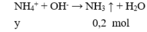
→ y = 0,2 (4)
Từ (1); (2); (3); (4) có x = y = 0,2; z = 0,1; t = 0,1.
Tổng khối lượng muối trong 300ml dung dịch là:
m = 3. (0,2.23 + 0,2.18 + 0,1.60 + 0,1.96) = 71,4 gam.

Đáp án : A
Trong 100 ml X : nCO3 = nCO2 = 0,1 mol
, mkết tủa = mBaCO3 + mBaSO4 = 43 => nSO4 = 0,1 mol
Trong 200 ml X : nNH3 = nNH4 = 0,4 mol
=> Trong 300 ml X có : 0,3 mol CO32- ; 0,3 mol SO42- ; 0,6 mol NH4+ và 0,6 mol Na+ ( BT điện )
=> mmuối = 71,4g

Chọn đáp án C
Xét trong 100 ml dung dịch X: 2H⁺ + CO32– → CO2 + H2O ⇒ nCO32– = nkhí = 0,1 mol.
Ba2+ + CO32– → BaCO3 || Ba2+ + SO42– → BaSO4 ⇒ nSO42– = (43 - 0,1 × 197) ÷ 233 = 0,1 mol.
NH4+ + OH– → NH3 + H2O ⇒ nNH4+ = nNH3 = 0,4 ÷ 2 = 0,2 mol.Bảo toàn điện tích: nNa+ = 0,2 mol.
⇒ mmuối trong 300ml X = 3 × (0,2 × 23 + 0,2 × 18 + 0,1 × 60 + 0,1 × 96) = 71,4(g) ⇒ chọn C.
Đáp án D
Qui đổi : X + NaOH = (NH3 + H3PO4) + NaOH
Có : nNaOH = 3nH3PO4 => nH3PO4 = 0,1 mol
nNH3 = 0,275 mol
Các phản ứng có thể xảy ra :
3NH3 + H3PO4 -> (NH4)3PO4 (1)
2NH3 + H3PO4 -> (NH4)2HPO4 (2)
NH3 + H3PO4 -> NH4H2PO4 (3)
Bảo toàn khối lượng : mmuối = mNH3 + mH3PO4 = 14,475g