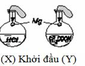
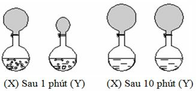
Hai bình như nhau, bình X chứa 0,5 lít axit clohiđric 2M, bình Y chứa 0,5 lít axit axetic 2M, được bịt kín bởi 2 bóng cao su như nhau. Hai mẩu Mg khối lượng như nhau được thả xuống cùng một lúc. Kết quả sau 1 phút và sau 10 phút (phản ứng đã kết thúc) được thể hiện như ở hình dưới đây:
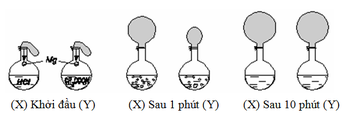
Cho các phát biểu sau:
(1) Sau 1 phút, khí
H
2
thoát ra ở bình X nhiều hơn ở bình Y.
(2) Sau 1 phút, khí
H
2
thoát ra ở bình Y nhiều hơn ở bình X.
(3) Sau 1 phút, khí
H
2
thoát ra ở 2 bình X và Y bằng nhau.
(4) Sau 10 phút, khí
H
2
thoát ra ở 2 bình X và Y bằng nhau.
(5) Sau 10 phút, khí
H
2
thoát ra ở 2 bình X nhiều hơn ở bình Y.
(6) Sau 1 phút hay sau 10 phút, khí
H
2
thoát ra luôn bằng nhau.
Các phát biểu đúng đúng là
A. (1), (4), (5).
B. (2), (4), (5), (6).
C. (1), (4).
D. (3), (4), (6).




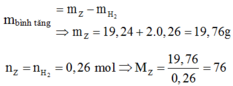


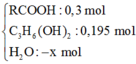

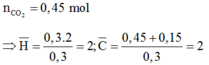

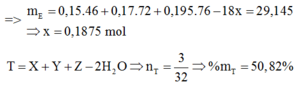
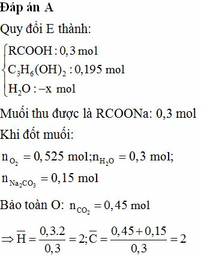


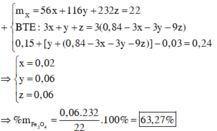


Chọn đáp án C.