Điện phân dung dịch chứa hỗn hợp CuSO4 và KCl với điện cực trơ đến khi thấy khí bắt đầu thoát ra ở cả hai điện cực thì dừng lại thấy có 448 ml khí (đktc) thoát ra ở anot. Dung dịch sau điện phân có thể hoà tan tối đa 0,8 gam MgO. Khối lượng dung dịch sau điện phân đã giảm bao nhiêu gam (coi lượng H2O bay hơi là không đáng kể) ?
A. 2,7
B. 1,03
C. 2,95
D. 2,89


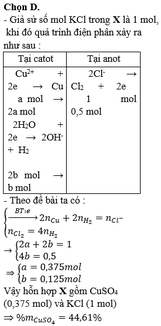

Chọn C
n(MgO) = 0,02; n(khí) = 0,02
Dung dịch sau điện phân có thể hòa tan MgO → có H2SO4
PTHH:
CuSO4 + 2KCl → Cu + Cl2 + K2SO4 1
x---------------------------- x mol
CuSO4 + H2O → Cu + H2SO4 + ½ O2 2
y------------------------------y ----------- y/2 mol
H2SO4 + MgO → MgSO4 + H2O
0,02 -------- 0,02 mol
Ta có hệ phương trình
1 n(khí) = x + y/2 = 0,02
2 n(H2SO4) = y = 0,02
Giải 1 2 có x = 0,01; y = 0,02
→ m(dung dịch giảm) = m(Cu) + m(Cl2) + m(O2) = 2,95 gam