Theo tiêu chuẩn Việt Nam, nồng độ cho phép của ion Cu2+ trong nước uống không được vượt quá 3mg/l. Khi cho dung dịch H2S dư vào 500ml 1 mẫu nước, lượng kết tủa tối thiểu là bao nhiêu cho thấy mẫu nước đã bị nhiễm đồng?
A. 0,00144
B. 0,00229
C. 0,00115
D. 0,0028


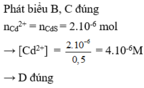
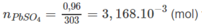
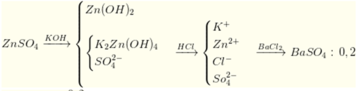


Đáp án B
Cu2+ + H2S → CuS + 2H+
Nồng độ CuS < 3mg/l
⇒ Trong 500ml mẫu nước nCuS < 3/64. 0,5= 0,0234 mmol = 0,0000234mol
⇒ mCuS <0,0000234 . 98 = 0,00229g
Vậy lượng kết tủa tối thiểu cho thấy mẫu nước đã nhiễm đồng là 0,0023mg