Bài 1: Cho 12 gam hỗn hợp X gồm Fe và Cu tác dụng với dung dịch H2SO4 loãng dư ,thu được 2,24lít khí H2 (đktc).Tính thành phần phần trăm mỗi kim loại trong hỗn hợp X.
Bài 2: Cho 13 gam kẽm tác dụng với axit clohidric, thu được V lít khí (đktc). Tính V?



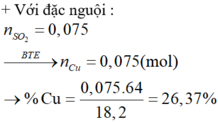

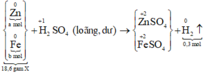
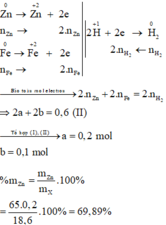
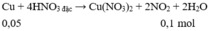
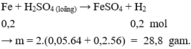

Câu 1:
\(n_{H_2}=\dfrac{2,24}{22,4}=0,1\left(mol\right)\\ PTHH:Fe+H_2SO_4\rightarrow FeSO_4+H_2\\ \Rightarrow n_{Fe}=0,1\left(mol\right)\\ \Rightarrow m_{Fe}=0,1\cdot56=5,6\left(g\right)\\ \Rightarrow\%_{Fe}=\dfrac{5,6}{12}\cdot100\%\approx46,67\%\\ \Rightarrow\%_{Cu}\approx100\%-46,67\%=53,33\%\)
Bài 2:
\(n_{Zn}=\dfrac{13}{65}=0,2\left(mol\right)\\ PTHH:Zn+2HCl\rightarrow ZnCl_2+H_2\\ \Rightarrow n_{H_2}=n_{Zn}=0,2\left(mol\right)\\ \Rightarrow V=V_{H_2\left(đktc\right)}=0,2\cdot22,4=4,48\left(l\right)\)