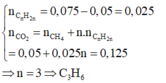chia 9,84gam hỗn hợp khí X gồm etilen và 1 hidrocacbon mạch hở A thành 2 phần bằng nhau.
Dẫn phần I qua dd brom dư,sau khi phản ứng kết thúc có V lít khí A thoát ra,khối lượng brom đã tham gia phản ứng là 8gam.
Đốt cháy hoàn toàn phần II rồi cho toàn bộ sản phẩm cháy vào bình chứa có 500ml dd Ba(OH)2 0,66M.Sau khi phản ứng kết thúc thu đc 63,04gam kết tủa.Dung dịch sau khi lọc bỏ kết tủa bị giảm đi m gam so với khối lượng của dd Ba(OH)2 ban đầu
a)Viết các phương trình hóa học và xác định công thức phân tử của A
b)Tính giá trị m và giá trị của V(đktc)