Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

bài 1
a. -hòa tan 3 kl trên vào dd NaOH dư
+tan => Al
2NaOH +2 Al + 2H2O => 2NaAlO2 + 3H2
+ko tan => Fe,Cu
- hòa tan 2 kim loại trên trong HCl dư
+tan => Fe
Fe + 2HCl=> FeCl2 + H2
+ko tan => Cu
b.
hòa tan hh trên vào NaOH dư
+tan => Al
+ko tan => Fe,Ag
-hòa tan 2 KL còn lại trong HCl
+tan=> Fe
+ko tan=> Ag
câu C
hòa tan các KL trên vào nước
+tan, có khí thoát ra => Na
Na + H2O =>. NaOH + 1/2H2
+ko tan => Al,Fe,Cu
hòa tan 3 kl còn lại trong NaOH dư
+tan => Al
+ko tan => Fe,Cu
hòa tan 2 kl còn lại vào HCl dư
+tan => Fe
+ko tan =.> Cu
câu d
hòa tan hh trên trong NaOh dư
+tan ,có khí => Al
NaOh + Al + H2o => NaAlO2 + 3/2H2
+tan => Al2O3
2NaOh + Al2o3 => 2NaAlO2 + H2O
+ko tan => Mg

a) Vì: mA < 400 (g) nên phải có khí thoát ra → muối có dạng MHSO4 và khí là: CO2
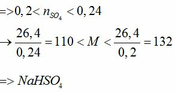
b)
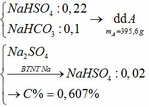
c) Tác dụng được với: MgCO3, Ba(HSO3)2, Al2O3, Fe(OH)2, Fe, Fe(NO3)2
Pt: 2NaHSO4 + MgCO3 → Na2SO4 + MgSO4 + CO2↑ + H2O
2NaHSO4 + Ba(HSO3)2 → BaSO4 + Na2SO4 + SO2↑ + 2H2O
6NaHSO4 + Al2O3 → 3Na2SO4 + Al2(SO4)3 + 3H2O
2NaHSO4 + Fe(OH)2 → Na2SO4 + FeSO4 + 2H2O
2NaHSO4 + Fe → Na2SO4 + FeSO4 + H2↑
12NaHSO4 + 9Fe(NO3)2 → 5Fe(NO3)3 + 2Fe2(SO4)3 + 6Na2SO4 + 3NO↑ + 6H2O

1. Cho các dãy các chất: CO2, MgCl2, HNO3, Na2SO4. Số chất trong dãy phản ứng được với dung dịch Ba(OH)2 là:
A.3 B.5 C.4 D.2
2. Cho 1,37g Ba vào 1 lít dung dịch CuSO4 0,01M. Sau khí các phản ứng xảy ra hoàn toàn, khối lượng kết tủa thu được là:
A. 3,31g B. 0,98g C. 2,33g D. 1,71g
3. Kim loại Zn không phản ứng với dung dịch:
A. AgNO3 B. NaCl C. CuSO4 D. HCl
4. Dung dịch Na2CO3 tác dụng được với chất nào sau đây?
A. CaCl2 B. BaSO4 C. KCl D. Mg(OH)2
5. Cho kim loại Fe lần lượt vào các dung dịch: Cu(NO3)2, AlCl3, AgNO3, MgCl2. Số trường hợp xảy ra phản ứng hóa học:
A. 3 B. 4 C. 1 D. 2
6. Hòa tan hoàn toàn m gam Fe vào dung dịch HCl (dư), thu được 1,12 lít khí H2(đktc). Giá trị của m là:
A. 2,8 B. 11,2 C. 5,6 D. 8,4
7. Viết các PTHH để thực hiện sơ đồ chuyển hóa sau:
Fe(OH)3 -> Fe2O3 -> Fe -> FeSO4 -> FeCl2 -> Fe(OH)2
Giải:
(1) : \(2Fe\left(OH\right)_3\rightarrow Fe_2O_3+3H_2O\)
(2): \(Fe_2O_3+3CO\rightarrow2Fe+3CO_2\)
(3): \(Fe+H_2SO_4\rightarrow FeSO_4+H_2\)
(5): \(FeSO_4+BaCl_2\rightarrow FeCl_2+BaSO_4\downarrow\)
(6): \(FeCl_2+2NaOH\rightarrow Fe\left(OH\right)_2+2NaCl\)
8. Hòa tan hoàn toàn 11,1 gam hỗn hợp X gồm Al và Fe bằng một lượng dư dung dịch HCl, thu được 6,72 lít khí H2(đktc).
a. Viết PTHH của các phản ứng xảy ra và tính phần trăm khối lượng của từng chất trong X
Giải:
Gọi x, y lần lượt là số mol Al và Fe
\(\rightarrow\) 27x+56y=11,1 (1)
\(2Al+6HCl\rightarrow2AlCl_3+3H_2\)
x mol_________\(\rightarrow\)________ \(\frac{3}{2}x\) mol
\(Fe+2HCl\rightarrow FeCl_2+H_2\)
y mol ________\(\rightarrow\) _______y mol
\(\rightarrow\) \(n_{H2}=\frac{3}{2}x+y\)
\(\Rightarrow\frac{3}{2}x+y=\frac{6.72}{22.4}\) (2)
Từ (1) và (2), Giải HPT, ta được:
\(\left\{{}\begin{matrix}x=0.1mol\\y=0.15mol\end{matrix}\right.\)
\(\Rightarrow\left\{{}\begin{matrix}mAl=27\cdot0.1=2.7\left(g\right)\\mFe=56\cdot0.15=8.4\left(g\right)\end{matrix}\right.\)
\(\Rightarrow\%mAl=\frac{2.7}{11.1}\cdot100=24.32\%\)
\(\Rightarrow\%mFe=100-24.32=75.68\%\)

Al + H2SO4 đặc nguội --> x
2Al + 3H2SO4 loãng --> Al2(SO4)3 + 3H2
2Al + 3Cl2 --to--> 2AlCl3
Al + 3AgNO3 --> Al(NO3)3 + 3Ag
Al + MgSO4 --> x
2Al + 2NaOH + 2H2O --> 2NaAlO2 + 3H2
=> B

Tính hoạt động kim loại: Mg > Fe > Cu > Ag
=> Hỗn hợp A:
+ 3 kim loại: Ag, Cu, Fe(dư)
+ 2 dung dịch: Mg(NO3)2 và Fe(NO3)2
\(Mg+2AgNO_3\rightarrow Mg\left(NO_3\right)_2+2Ag\\ Mg+Cu\left(NO_3\right)_2\rightarrow Mg\left(NO_3\right)_2+Cu\\ Fe+2AgNO_3\rightarrow Fe\left(NO_3\right)_2+2Ag\\ Fe+Cu\left(NO_3\right)_2\rightarrow Fe\left(NO_3\right)_2+Cu\)
Tách riêng kim loại: Cho hỗn hợp tác dụng với dung dịch HCl dư, lấy phần dung dịch tác dụng hết với dung dịch NaOH dư, lọc lấy kết tủa đem nung ngoài không khí tới khối lượng không đổi.
Cho luồng H2 nóng dư đi qua thu được Fe tinh khiết
\(Fe+2HCl\rightarrow FeCl_2+H_2\\ NaOH+HCl\rightarrow NaCl+H_2O\\ 2NaOH+FeCl_2\rightarrow Fe\left(OH\right)_2\downarrow+2NaCl\\ 4Fe\left(OH\right)_2+O_2\rightarrow2Fe_2O_3+4H_2O\\ 3H_2+Fe_2O_3\rightarrow2Fe+3H_2O\)
(Tách Fe)
Phần chất rắn nung trong không khí tới khối lượng không đổi, cho tác dụng với dung dịch HCl dư lọc lấy kết tủa sấy khô thu được Ag tinh khiết.
\(2Cu+O_2\underrightarrow{^{to}}2CuO\\ CuO+2HCl\rightarrow CuCl_2+H_2O\)
Phần dung dịch cho tác dụng với dung dịch NaOH dư lấy kết tả nung trong không khí tới khối lượng không đổi thu được chất rắn rồi cho luồng H2 nóng dư đi qua thu được Cu tinh.
\(NaOH+HCl\rightarrow NaCl+H_2O\\ 2NaOH+CuCl_2\rightarrow Cu\left(OH\right)_2\downarrow+2NaCl\\ H_2+CuO\underrightarrow{^{to}}Cu+H_2O\)



1D
`Fe + Cu(NO_3)_2 -> Fe(NO_3)_2 + Cu`
`Fe + 2AgNO_3 -> Fe(NO_3)_2 + 2Ag`
2B
3A
`Na_2CO_3 + CaCl_2 -> CaCO_3 + 2NaCl`