Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Xác định thành phần của hỗn hợp khí :
- Số mol CO 2 có trong hỗn hợp được tính theo (1) :
n CO 2 = n CaCO 3 = 1/100 = 0,01 mol
- Số mol CO có trong hỗn hợp được tính theo (2) :
n CO = n Cu = 0,64/64 = 0,01
Thành phần phần trăm theo thể tích của hỗn hợp khí được tính theo số mol của mỗi khí. Ta có kết quả : Hỗn hợp khí có 50% thể tích của mỗi khí.

Gọi số mol của CH4 và C2H2 lần lượt là a và b
CH4 + 2O2 ➝ CO2 + 2H2O
a 2a a
C2H2 + 2,5O2 ➝ 2CO2 + H2O
b 2,5b 2b
CO2 + Ca(OH)2 ➝ CaCO3 + H2O
a + 2b a + 2b
Số mol của hỗn hợp khí: a + b = 4,48/22,4 = 0,2 mol
Số mol kết tủa: a + 2b = 30/100 = 0,3 mol
➝ a = 0,1 mol, b = 0,1 mol
a) %VC2H2 = %VCH4 = 50%
b) Tổng số mol khí O2 đã dùng: a + 2,5b = 0,35 mol
➝ VO2 = 0,35.22,4 = 7,84 lít
➝ V kk = 5.VO2 = 39,2 lít

a) Gọi số mol CH4, C2H2 là a, b (mol)
=> \(a+b=\dfrac{4,48}{22,4}=0,2\) (1)
\(n_{CaCO_3}=\dfrac{30}{100}=0,3\left(mol\right)\)
PTHH: CH4 + 2O2 --to--> CO2 + 2H2O
a--->2a----------->a
2C2H2 + 5O2 --to--> 4CO2 + 2H2O
b------>2,5b-------->2b
Ca(OH)2 + CO2 --> CaCO3 + H2O
0,3<-----0,3
=> a + 2b = 0,3 (2)
(1)(2) => a = 0,1 (mol); b = 0,1 (mol)
=> \(\%V_{CH_4}=\%V_{C_2H_2}=\dfrac{0,1}{0,2}.100\%=50\%\)
b) nO2 = 2a + 2,5b = 0,45 (mol)
=> VO2 = 0,45.22,4 = 10,08 (l)
=> Vkk = 10,08.5 = 50,4 (l)

\(n_{CaCO3}=\dfrac{2}{100}=0,02\left(mol\right)\)
Bảo toàn nguyên tố C: \(n_{CO}=n_{CaCO_3}=0,02\left(mol\right)\)
\(n_{Cu}=\dfrac{1,92}{64}=0,03\left(mol\right)\)
CuO + CO -------> Cu + CO2
0,02-------->0,02-->0,02
CuO + H2 -------> Cu + H2O
0,01<--------0,03-0,02=0,01
Phần trăm về thể tích cũng là phần trăm về số mol
=>\(\%V_{H_2}=\dfrac{0,01}{0,01+0,02}.100=33,33\%\)
=> %VCO=100- 33,33=66,67%
\(\%m_{H_2}=\dfrac{2.0,01}{2.0,01+44.0,02}.100=2,22\%\)
%mCO= 100-2,22=97,78%
b) \(V_{CO_2}=0,02.22,4=0,448\left(l\right)\)

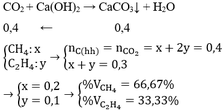


a) Khi đi vào dd Ca(OH)2 dư thì chỉ có CO2 phản ứng
CO2 + Ca(OH)2 --> CaCO3↓ + H2O
nCaCO3 = 1/100 = 0,01 mol = nCO2
Khi đi qua CuO dư đun nóng thì chỉ có CO phản ứng
CO + CuO --> CO2 + Cu
nCu = 0,64/64 = 0,01 mol = nCO
b) vậy hỗn hợp gồm CO và CO2 đều có số mol là 0,01 mol
=> % V mỗi khí = 50%
c) 2CO + O2 --> 2CO2
=> nO2 = \(\dfrac{nCO}{2}\)= 0,05 mol
=> Thể tích khí oxi cần dùng để đốt cháy hỗn hợp CO và CO2 là 0,05.22,4 = 1,12 lít.